下列关于营养物质的说法正确的是 ( )
| A.油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物 |
| B.1mol蔗糖的水解产物是1mol葡萄糖和1mol果糖 |
| C.淀粉溶液和稀硫酸共热后发生水解反应,冷却后加少量银氨溶液,水浴加热后会出现光亮的银镜 |
| D.鸡蛋白溶液中滴加饱和的硫酸铵溶液,出现白色沉淀,该过程叫做蛋白质的变性 |
右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是( )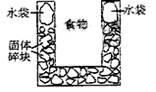
| A.硝酸铵 | B.氯化镁 | C.食盐 | D.生石灰 |
美国《科学》杂质评选的2001年十大科学进展之一是国际气候变化研究专家组首次正式表明,过去50年中的全球变暖现象很可能是由大气中的温室气体如CO2聚集造成的。科学家对此问题提出了一些设想,有科学家提出可以将CO2通过管道输送到海底,这样可减缓空气中CO2浓度的增加。下列有关说法不正确的是( )
| A.送到海底越深的地方,CO2溶解得越多,同时CO2可能液化甚至变成干冰 |
| B.把CO2输送到海底,会使海水酸性增强,破坏海洋生态环境 |
| C.把CO2输送到海底,这是人类减缓空气中CO2浓度的增加的唯一办法 |
| D.要减缓空气中CO2浓度的增加,最有效的措施是使用新能源,植树造林等 |
将氯化铝溶液和氢化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是()
①1:3②2:3③1:4④2:7⑤任意比
| A.②③ | B.只有⑤ | C.②④ | D.①④ |
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
下列推断不合理的是()
| A.直接蒸干滤液得到纯净的(NH4)2SO4 |
| B.生成1mol(NH4)2SO4至少2molNH3 |
| C.CO2可被循环使用 |
| D.往甲中通适量CO2有利于(NH4)2SO4生成 |
为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是()
A.氢氧化钠是否 变质(BaC12) 变质(BaC12) |
B.FeSO4是否被氧化(KSCN) |
| C.KI是否被氧化(淀粉溶液) | D.K2SO3是否被氧化(BaC12) |