三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2。其反应原理为:
下列说法正确的是
| A.反应①是氧化还原反应 |
| B.反应②中HNCO是氧化剂 |
| C.反应②中,每转移1mol电子,消耗NO20.25 mol |
| D.反应②中氧化剂、还原剂的物质的量之比为4∶3 |
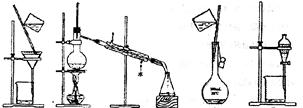
以下实验装置可用于分离沸点相差较大的液体互溶物的是 ()
()
AB CD
下列各组混合物中,能用分液漏斗分离的是()
| A.酒精和水 | B.碘和四氯化碳 | C.水和四氯化碳 | D.汽油和植物油 |
下列仪器不能用于加热的是( )
)
| A.试管 | B.烧杯 | C.量筒 | D.坩埚 |
以下是一些常用的危险品标志,装运乙醇(酒精)的包装箱应贴的图标是()
两种气态烃以任意比例混合,在105℃时,1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积为10L。下列各组混合烃中不符合此条件的是
①CH4、C2H4 ② CH4、C3H6 ③ C2H4、C3H4 ④ C2H2、C3H6
| A.没有 | B.只有②④ | C.①②④ | D.②③④ |