实验是化学研究的基础,关于下列各装置图的叙述中,正确的是 网
网
A.装置①是一套实验室制气装置,用于发生、干燥和收集气体,如铜屑与稀硝酸 |
B.装置②中,a为正极,d为阳极 |
C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等 |
D.装置④能用于测量气体体积的装置 |
下列实验方案正确且能达到相应实验预期目的的是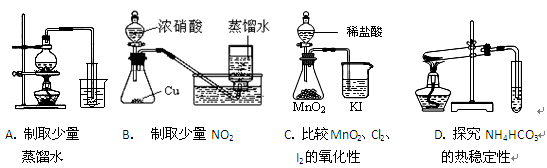
已知:N2(g)+3H2(g) 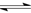 2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 |
容器1 |
容器2 |
| 反应物投入量始态 |
1mol N2、3mol H2 |
2mol NH3 |
| NH3的平衡浓度/mol·L-1 |
cl |
c2 |
| 反应的能量变化 |
放出a kJ |
吸收b kJ |
| 体系压强/Pa |
p1 |
p2 |
| 反应物转化率 |
α1 |
α2 |
下列说法不正确的是()
A. cl 一定等于c2 B.a + b = 92.4
C. p1 一定等于p2 D.α1 一定等于α2
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是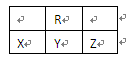
| A.X的氢化物比R的氢化物稳定 |
| B.原子半径大小顺序是Z>Y>X |
| C.Y、R形成的化合物YR2能使KMnO4溶液褪色 |
| D.X、Z可形成化合物XZ5,分子中各原子均满足最外层8电子结构 |
下列有关平衡常数的说法正确的是
A.已知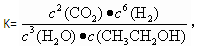 则对应的化学反应可以表示为: 则对应的化学反应可以表示为:2CO2(g) + 6H2(g) 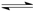 CH3CH2OH(g) + 3H2O(g) CH3CH2OH(g) + 3H2O(g) |
| B.将某浓度醋酸溶液升高温度,醋酸的电离平衡常数Ka将变大 |
| C.常温下,向纯水中加入少量碳酸钠固体,水的电离程度变大,Kw变大 |
D.常温下,在饱和氯水中加入少量碳酸钙固体,Cl2+H2O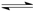 HCl+HClO平衡正移,平衡常数K变大 HCl+HClO平衡正移,平衡常数K变大 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2 SO3(g)△H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2 SO3(g)△H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是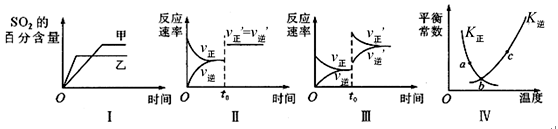
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |