Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应方程式为:2Cu+H2O==Cu2O+H2 。下列说法正确的是 ( )
。下列说法正确的是 ( )


A.石墨电极接直流电源的正极 |
B.铜电极发生的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O |
C.铜电极接直流电源的负极 |
D.当有0.1mol电子转移时,有0.1molCu2O生成。 |
某烃完全燃烧,生成的CO2和H 2O的物质的量之比2:1则该烃的分子式可能是( )
| A.CH4 | B.C2H4 | C.C3H8 | D.C6H6 |
一定温度下,反应A2(g)+B2(g) 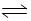 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
| A.单位时间内生成n molA2同时生成n molAB |
| B.单位时间内生成2n molAB的同时生成n molB2 |
| C.容器内气体总压强不再随时间的变化而变化 |
D.容器 内混合气体的平均摩尔质量不再随时间的变化而变化 内混合气体的平均摩尔质量不再随时间的变化而变化 |
下列说法正确的是()
| A.含有共价键的化合物一定是共价化合物,在共价化合物中一定含有共价键 |
| B.含有离子键的化合物一定是离子化合物,在离子化合物中可以含有非极性共价键 |
| C.非极性共价键只能存在于非金属单质中,不可能存在于化合物中 |
| D.不同元素原子形成的多原子分子中,含有的化学键只能是极性共价键 |
已知中和热的数值是57.3KJ/mol 。下列反应物混合时,产生的热量等于57.3KJ的是()
。下列反应物混合时,产生的热量等于57.3KJ的是()
| A.1mol/L盐酸和1mol/LNaOH溶液等体积混合 |
| B.500mL1.0mol/L的硫酸和500mL1.0mol/L的Ba(OH)2溶液 |
| C.500mL2.0mol/L的盐酸和500mL2.0mol/L的NaOH溶液 |
D.500mL2.0mol/L CH3COO H溶液和500mL2.0mol/L NaOH溶液 H溶液和500mL2.0mol/L NaOH溶液 |
元素A、B的原子序数都小于18,已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a一b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有 ( )
A.能与水反应 B.能与盐酸反应 C.能与NaOH溶液反应 D.能与硫酸钠反应