右图是实验室模拟煤的干馏的实验装置,下列有关叙述不正确的是( )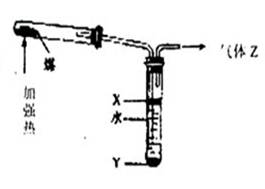
| A.图示实验中发生了化学反应实验后水溶液的Ph〉7, |
| B.溶液Y是黑色粘稠的煤焦油,上层X是粗苯等气体 |
| C.Z中有些成分易燃,且可以还原氧化铜溶液 |
| D.Y是一种纯净物 |
有关下图的说法不正确的是
| A.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+ |
| B.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| C.要使Fe极不被腐蚀,Cu片换Zn片或将a与直流电源的负极相连 |
| D.a和b分别连接直流电源正、负极,Fe片上有气体产生 |
已知常温下:Ksp(AgCl)=1.8×10-10 mol2·L-2,Ksp(Ag2CrO4)=1.9×10-12 mol3·L-3,
下列叙述正确的是
| A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr) |
| C.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl 和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀 |
| D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
反应:xA(气)+yB(气)  zC(气),达到平衡时测得A气体的浓度为0.5 mol·L-1,当在恒温下将该容器体积扩大一倍,再次达到平衡,测得A气体的浓度为0.3 mol·L-1,则下列叙述正确的是
zC(气),达到平衡时测得A气体的浓度为0.5 mol·L-1,当在恒温下将该容器体积扩大一倍,再次达到平衡,测得A气体的浓度为0.3 mol·L-1,则下列叙述正确的是
| A.C的质量分数降低 | B.平衡向右移动 |
| C.B的转化率升高 | D.x+y<z |
银锌电池的电极分别是Ag2O和Zn,电解质溶液为KOH,它的放电过程表示为:
Ag2O + Zn + H2O ═ 2Ag + Zn(OH)2,下列叙述,正确的是
| A.在放电过程中,Ag2O为负极 |
| B.在放电过程中,电池负极区溶液pH减小 |
| C.在放电过程中,电子由Ag2O经外电路流向Zn |
| D.放电时,Ag2O电极发生氧化反应,Zn极发生还原反应 |
下列叙述错误的是
| A.生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B.铁在潮湿空气中发生腐蚀,其负极反应是2H++2e-=H2↑ |
| C.用锡焊接的铁质器件,焊接处易生锈 |
| D.铁管上镶嵌锌块,铁管不易被腐蚀 |