物质的颗粒达到纳米级时,具有特殊的性质。如将单质铜制成“纳米铜”时,“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列叙述中正确的是
| A.常温下,“纳米铜”比铜片的金属性强 | B.常温下,“纳米铜”比铜片更易失电子 |
| C.常温下,“纳米铜”与铜片的还原性相同 | D.常温下,“纳米铜”比铜片的氧化性强 |
根据中学化学教材所附元素周期表,判断下列叙述不正确的是
| A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等 |
| B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等 |
| C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 |
| D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等 |
下列方程式书写正确的是
A.NaHCO3在水溶液中的电离方程式:NaHCO3 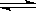 Na++HCO3- Na++HCO3- |
B.H2SO3的电离方程式H2SO3 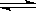 2H++SO32- 2H++SO32- |
C.CO32-的水解方程式:CO32-+2H2O 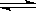 H2CO3+2OH- H2CO3+2OH- |
D.HS-的水解方程式:HS-+H2O 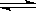 H2S+OH- H2S+OH- |
NA为阿伏伽德罗常数,下列叙述正确的是
| A.一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液含NH+4物质的量不同 |
| B.1L1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
| C.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子 |
| D.乙烯和环丙烷(C3H6)组成的28g混合气体中含有3NA 个氢原子。 |
下列说法中正确的是
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
| B.自发反应在恰当条件下才能实现 |
| C.高温高压下使石墨转化为金刚石的反应是自发的化学反应 |
| D.同一物质的固、液、气三种状态的熵值相同 |
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能
| A.③⑤⑥⑦⑧ | B.⑤⑥⑦⑧ | C.①②③④ | D.③④⑤⑥⑦⑧ |