在水中加入等物质的量的Na+、Ag+、Pb2+和SO42-、Cl-、NO3-,然后放入惰性材料做电极的电解槽中,通电片刻,则氧化产物与还原产物的质量比为:
A.35.5 :108 |
B.16 :207 |
C.8 :1 |
D.108 :35.5 |
浓硫酸和2 mol·L-1的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图。分析a、b曲线变化的原因是( )
| A.a升华、b冷凝 | B.a挥发、b吸水 |
| C.a蒸发、b潮解 | D.a冷凝、b吸水 |
为方便某些计算,有人将98%的浓硫酸表示成下列形式,其中合理的是( )
A.H2SO4· H2O H2O |
B.H2SO4·H2O |
| C.H2SO4·SO3 | D.SO3· H2O H2O |
储存浓H2SO4的铁罐外口出现严重的腐蚀现象,这体现了浓硫酸的( )
| A.脱水性和吸水性 | B.吸水性和酸性 |
| C.强氧化性和吸水性 | D.不挥发性和酸性 |
50 mL 18 mol·L-1的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量为 …
( )
| A.等于0.9 mol | B.大于0.45 mol,小于0.9 mol |
| C.等于0.9 mol | D.小于0.45 mol |
浓硫酸和2 mol·L-1的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如下图,分析a、b曲线变化的原因是( )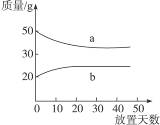
| A.a升华、b冷凝 | B.a挥发、b吸水 | C.a蒸发、b潮解 | D.a冷凝、b吸水 |