ClO2是一种消毒杀菌效率高,二次污染小的水处理剂。实验室可通过以下反应制得:
2KClO3+ H2C2O4+ H2SO4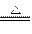 2ClO2 ↑+ K2SO4 + 2CO2↑+ 2H2O。下列说法正确的是:
2ClO2 ↑+ K2SO4 + 2CO2↑+ 2H2O。下列说法正确的是:
A.1mol KClO3参加反应有2mol电子转移 |
B.H2C2O4在反应中被还原 |
C.ClO2是氧化产物 |
D.等物质的量ClO2消毒杀菌的效率是等物质的量Cl2的2.5倍 |
下列各组物质中既不属同系物,又不属同分异构体的是()
| A.淀粉和纤维素 | B.硬脂酸甘油脂和醋酸甘油三酯 |
| C.甘氨酸和丙氨酸 | D.苯甲醇和邻甲基苯酚 |
1L0.1mol·L—1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发) ( )
| A.溶液的浓度变为0.08mol·L—1 | B.阳极上产生112mLO2(标准状况) |
| C.转移的电子数是l.204×1022个 | D.反应中有0.01mol的Ag被氧化 |
下列说法中正确的是
A.原子及其离子的核外电子层数等于该元素所在的周期数;
B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素;
C稀有气体原子的最外层电子数都是8;
D.同一元素的各种同位素的物理性质、化学性质均相同
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
下列叙述不正确的是( )
| A.放电时负极反应为:Zn-2e—+2OH—=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3 -3e—+ 5OH—=FeO42-+ 4H2O |
| C.放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A.X与Y形成化合物是,X可以显负价,Y显正价 |
| B.第一电离能可能Y小于X |
| C.最高价含氧酸的酸性:X对应的酸性弱于于Y对应的 |
| D.气态氢化物的稳定性:HmY小于HmX |