(1)卤素单质F2、Cl2、Br2、I2的熔沸点由高到低排列为 ,理由是 。卤化氢HF、HCl、HBr、HI中,沸点最低为 ,最高为 ,造成的原因为 。
(2)晶体硼的熔点和硬度都介于金刚石和晶体硅之间。
①晶体硼的晶体类型属于 晶体,理由是 。
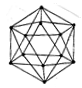 ②如图,晶体硼的基本结构单元都是硼原子组成的正二十面体,其中含
②如图,晶体硼的基本结构单元都是硼原子组成的正二十面体,其中含
有20个等边三角形和一定数目的顶角,每个顶角上各有一个硼原子,
观察此图,试回答:
这个基本结构单元由 个硼原子组成,键角是 ,
共含有 个B—B键。
现有三种常见治疗胃病药品的标签:
药品中所含的物质均能中和胃里过量的盐酸,关于三种药片中和胃酸的能力比较,正确的是
| A.①=②=③ | B.①>②>③ | C.③>②>① | D.②>③>① |
钠在干燥空气中形成的氧化物0.70 g,溶于水后,可被100 g质量分数为0.73%的盐酸恰好中和,钠的氧化物的成分是
| A.Na2O2和Na2O | B.Na2O | C.Na2O2 | D.无法确定 |
将m1 g锌加到m2 g 20%的HCl溶液中去,反应结果共放出n L 氢气(在标准状况下),则被还原的HCl的物质的量是
A. |
B. |
C.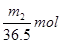 |
D.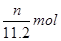 |
实验室有三瓶失去标签的试剂,分别是Na2CO3、NaCl、AgNO3。实验员选择了一种试剂就把它们区别开来了,这种试剂是:
| A.盐酸 | B.氢氧化钠溶液 | C.氯化钡溶液 | D.硝酸 |
既能与盐酸反应,又能与NaOH溶液反应的是
①Na2SiO3 ②Al(OH)3 ③SiO2 ④Al2O3 ⑤NaHCO3
| A.①②④ | B.②④⑤ | C.②③④ | D.全部 |