对下列事实的解释正确的是( )
| A.浓硝酸的光照下变黄,说明浓硝酸不稳定,且产物有红棕色气体可溶于浓硝酸。 |
B.向某溶液中加入氯化钡溶液和稀硝酸,有白色沉淀生成,说明该溶液中一定含有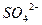 。 。 |
| C.常温下,将铜放入浓硫酸中无明显变化,说明铜在冷、浓硫酸中钝化。 |
| D.氯气使湿润的碘化钾淀粉试纸变蓝,说明氯气与淀粉反应。 |
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法正确的是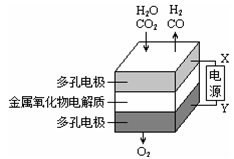
| A.X是电源的正极 |
| B.阴极的反应式是:H2O+2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ |
C.总反应可表示为:H2O+CO2 H2+CO H2+CO |
| D.阴、阳两极生成的气体的物质的量之比是1︰1 |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
中和滴定是一种操作简单、准确度高的定量分析方法。实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析,这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是
| A.用标准酸性KMnO4溶液滴定Na2SO3溶液以测定其浓度:KMnO4——紫红色 |
| B.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测定AgNO3溶液浓度:Fe(SCN)3——红色 |
| C.利用“2Fe3++2I-===I2+2Fe2+”,用FeCl3溶液测量KI样品中KI的百分含量:淀粉——蓝色 |
| D.利用OH-+H+===H2O来测量某盐酸的浓度时:酚酞——浅红色 |
如图曲线a和b是盐酸与氢氧化钠相互滴定的滴定曲线,下列叙述正确的是
| A.盐酸的物质的量浓度为1 mol·L-1 |
| B.P点时恰好完全反应,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠的滴定曲线 |
| D.酚酞不能用作本实验的指示剂 |
下列操作,妥当的是
| A.用托盘天平称量氢氧化钠固体时,需在左、右托盘上各放一块质量相等的滤纸 |
| B.用25 mL滴定管量取25 mL的氢氧化钠溶液时,需将调好零点的滴定管内所有液体放出 |
| C.用25 mL滴定管量取10 mL氢氧化钠溶液时,下端玻璃导管尖嘴悬挂的液滴不需处理 |
| D.用量筒量取一定量体积的液体配制一定物质的量浓度的溶液时,不需把蒸馏水洗涤量筒后的洗涤液移入容量瓶 |