下列离子方程式正确的是( )
A.H2O2 + 2OH-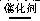 2H2O + O2↑ 2H2O + O2↑ |
B.2MnO4- + H2O2 + 6H+ = 2Mn2+ + 3O2↑+ 4H2O |
| C.2Fe3++H2S=2Fe2++S↓+2H+ | D.3ClO- + 2Fe(OH)3 = 2FeO42- + 3Cl- + H2O + 4H+ |
有甲、乙、丙、丁四种金属,将甲、乙用导线相连放入稀硫酸中可以看到乙慢慢溶解,而甲的表面有气泡逸出;把丁放在乙的硝酸盐溶液中后,丁表面覆盖一层乙的单质;用石墨电极电解含有相同物质的量浓度的甲和丙两种金属的盐溶液,丙的单质先析出;将甲放入稀盐酸中有H2析出。已知四种金属中有一种是铜,根据以上实验判断铜是()
| A.甲 | B.乙 | C.丙 | D.丁 |
用石墨作电极电解100 mL H2SO4与CuSO4的混合液,通电一段时间后,两极均收集到2.24 L(标准状况)气体,则原混合液中Cu2+的物质的量浓度为()
| A.1 mol·L-1 |
| B.2 mol·L-1 |
| C.3 mol·L-1 |
| D.4 mol·L-1 |
如图4-18所示,3个电解装置中都盛有相同体积和相同物质的量浓度的CuSO4溶液,通电一段时间并且通过相同的电量时,CuSO4溶液的物质的量浓度的大小关系正确的是()
图4-18
| A.①>②>③ |
| B.②>③>① |
| C.②=③>① |
| D.①=②=③ |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A.准状况下的22.4 L辛烷完全燃烧,生成二氧化碳分子数为8NA |
| B.18 g水中含有的电子数为10NA |
| C.46 g二氧化氮和46 g四氧化二氮含有的原子数均为3NA |
| D.在1 L 2 mol·L-1的氢氧化铁溶胶中含有氢氧化铁胶粒数为2NA |
下列判断正确的是()
①分散系一定是混合物②浊液可用过滤的方法分离③任何物质在水中都有一定的溶解度④任何溶胶加入可溶性电解质后都能使胶体粒子聚沉成较大颗粒而形成沉淀析出⑤丁达尔效应、布朗运动而电泳现象都是胶体的物理性质⑥因为胶粒比溶液中溶质粒子大,所以可以用过滤的方法把胶粒分离出来⑦饱和溶液一定比不饱和溶液浓⑧相同条件下,相同溶质的溶液,饱和溶液要比不饱和溶液浓些
| A.①⑤⑧ |
| B.②④⑥⑧ |
| C.①②③④ |
| D.全部正确 |