汽车的启动电源常用铅蓄电池,放电时的电池反应如下:
PbO2 + Pb + 2H2SO4 = 2PbSO4↓ + 2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 | B.负极的电极反应式为:Pb + SO – 2e – = PbSO4↓ – 2e – = PbSO4↓ |
| C.PbO2得电子,被氧化 | D.电池放电时,溶液酸性增强 |
下列说法不正确的是
| A.金属单质与盐溶液的反应都是置换反应 |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3属于化合反应 |
| C.SO2+Cl2+2H2O=2HCl+H2SO4属于氧化还原反应 |
| D.AgNO3+HCl=AgCl↓+HNO3该反应不能说明盐酸酸性比硝酸强 |
某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO- 离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
| A.Na+ | B.CO32-、NH4+ |
| C.CH3COO- | D.CH3COO-、Na+ |
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO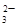 、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
| A.Cu2+、H+、Cl- | B.K+、OH-、CO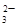 |
| C.K+、H+、Cl- | D.CO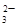 、OH-、Cl- 、OH-、Cl- |
下列各组离子一定能大量共存的是
A.某无色透明的酸性溶液:Cl-、Na+、MnO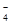 、 、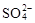 |
B.能使pH试纸变深蓝色的溶液:Na+、 、K+、 、K+、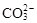 |
C.加入过量NaOH溶液后可得到澄清的溶液:K+、Ba2+、HCO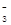 、Cl- 、Cl- |
D.常温下PH=12的溶液:K+、Ba2+、Cl-、NO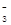 |
下列各组离子中,因发生氧化还原反应而不能大量共存的是
A.Fe3+、H+、SO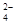 、ClO- 、ClO- |
B.Fe3+、Fe2+、SO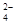 、OH- 、OH- |
C.Al3+、Na+、SO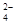 、HCO3- 、HCO3- |
D.K+、H+、I-、MnO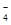 |