用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A.60.0g水晶晶体中,含有“Si—O”键的数目为NA |
| B.34g过氧化氢分子中可以形成极性共价键的数目为NA |
| C.状况下,22.4L甲烷和氨气的混合气体所含有的电子总数约为10NA |
| D.1molT2气体分子(超重氢分子)中所含的中子总数为2NA |
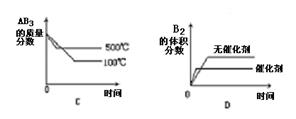
对于可逆反应:A2(g)+3B2(g) 2AB3(g) △H>0下列图象中正确的是
2AB3(g) △H>0下列图象中正确的是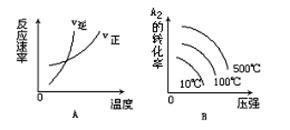
如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是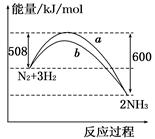
A.该反应的热化学方程式为: N2+3H2 2NH3 ΔH=-92 kJ/mol 2NH3 ΔH=-92 kJ/mol |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
下列有关热化学方程式的叙述中,正确的是
| A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,该反应的热化学方程式是 NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=+57.4 kJ·mol-1 |
| B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石一定比石墨稳定 |
| C.已知2H2O(g)=2H2(g)+O2(g) △H=+483.6 kJ·mol-1,则提供483.6 kJ热量时,一定会使2 mol H2O (g)发生分解 |
| D.已知C(s)+O2(g)=CO2(g) △H=a kJ·mol-1,2C(s)+O2(g)=2CO(g),△H=b kJ·mol-1,则2CO(g)+O2(g)=2CO2(g) △H=(2a﹣b) kJ·mol-1 |
下列关于电解精炼铜的叙述中不正确的是
| A.粗铜板为阳极 |
| B.粗铜所含Au、Ag、Fe、Zn等杂质,电解后以单质形式沉积槽底,形成阳极泥 |
| C.电解时,阳极发生氧化反应,而阴极发生的反应为Cu2++2e-=Cu |
| D.精铜的纯度可达99.95%~99.98% |
某同学为完成 2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验如图所示你认为可行的是