化合物丙由如下反应得到: ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 |
| C.CH3CHBrCHBrCH3 | D.(CH3)2CBrCH2Br |
反应A(g)+B(g) C(g) +D(g)发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是
C(g) +D(g)发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是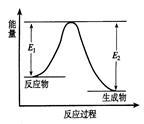
| A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大 |
| B.反应体系中加入催化剂,反应速率增大,△H不变 |
| C.△H < 0,反应达到平衡时,升高温度,A的转化率增大 |
| D.△H > 0,反应达到平衡时,升高温度,A的转化率减少 |
最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1molN-N吸收193kJ热量,生成1molN≡N放出941kJ热量。根据以上信息和数据,下列说法正确的是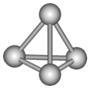
| A.N4属于一种新型的化合物 |
| B.N4是N2的同系物 |
| C.N4转变为N2是物理变化 |
| D.1molN4气体转变为N2放出724kJ能量 |
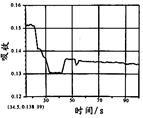
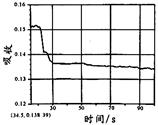
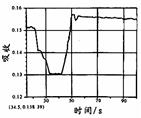
在图1所示密闭容器中充满红棕色的NO2气体,当迅速将活塞向右推一段距离后保持活塞不动时,色度计测出颜色变化的情况如图2所示。如果迅速将活塞往左拉一段距离后保持活塞不动时,色度计测出颜色变化的情况正确的图示为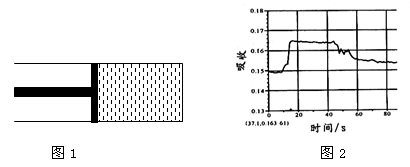
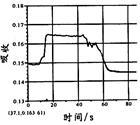 |
 |
 |
 |
| A. |
B. |
C. |
D. |
化学与人类生产、生活密切相关,下列有关说法正确的是
| A.工业上用惰性电极电解熔融的MgO可制得Mg |
| B.氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 |
| C.草木灰可与铵态氮肥混合施用 |
| D.为加快漂白精的漂白速率,使用时可滴加几滴醋酸 |
有人设计将两根铂丝做电极插入到KOH溶液中,然后在两极上分别通入甲烷和氧气而构成燃料电池。该电池中反应的化学方程式为CH4+2O2+2KOH K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是 (已知1个电子所带电量为1.6×10-19C)
K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是 (已知1个电子所带电量为1.6×10-19C)
A.通入甲烷的电极为电池的负极,通入氧气的电极为正极
B.在标准状况下,每消耗5.6 L O2,可向外提供2.4×104 C的电量
C.通入甲烷电极的电极反应为:CH4+10OH--8e- CO32-+7H2O
CO32-+7H2O
D.放电一段时间后,溶液的pH减小