把一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体Y 33.6L(在标准状况下.)。将反应后的溶液稀释到1 L,测得溶液的pH=1,则下列叙述错误的是( )
| A.气体Y的平均相对原子质量是14.4 | B.气体Y中SO2和H2的体积比为1:4 |
| C.反应中共消耗锌87.5g | D.反应中共转移电子3 mol |
实验室可用NaNO2+NH4Cl =NaCl+N2↑+2H2O制备N2,下列说法正确的是
| A.NaNO2发生氧化反应 |
| B.NH4Cl中的氮元素被还原 |
| C.N2既是氧化产物,又是还原产物 |
| D.每生成1mol N2转移电子的物质的量为6mol |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0 mol·L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- |
| B.c(H+)/ c (OH—)=10-10的溶液:K+、Ba2+、NO3-、Cl- |
| C.pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- |
| D.c(ClO-)=1.0 mol·L-1的溶液:Na+、SO32-、S2-、SO42- |
下列表述正确的是
| A.中子数为10的氧原子:18 10O |
B.Na2S的电子式: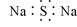 |
| C.聚氯乙烯的结构简式:CH2CHCl |
| D.Mg5(Si4O10)2(OH)2·4H2O的氧化物形式:5MgO·8SiO2·5H2O |
化学与材料、生活和环境密切相关。下列有关说法中错误的是
| A.新型材料聚酯纤维、光导纤维都属于有机高分子 |
| B.医药中常用酒精来消毒,是因为酒精能够使细菌蛋白发生变性 |
| C.大力实施矿物燃料脱硫脱硝技术以减少硫、氮氧化物排放 |
| D.煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 |
已知:还原性HSO—3>I—,氧化性IO—3>I2。在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是
| A.0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ |
| B.a点时消耗NaHSO3的物质的量为0.12mol |
| C.当溶液中I—与I2的物质的量之比为5:2时,加入的KIO3为0.18mol |
| D.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 |