某同学按下列操作进行实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度均为0.1mol/L的KBr、KI(含淀粉)、NaOH(含酚酞)、FeSO4(含KSCN)溶液各一滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图),在圆心处放置2粒芝麻大小的KClO3晶体,向KClO3晶体滴加一滴浓盐酸,(ClO3—+5Cl—+6H+=3Cl2↑+3H2O),立即将表面皿盖好,有关反应的现象或对应的氧化还原反应的离子方程式不正确的是( )
| A.a处溶液显黄色:2Br—+Cl2=2Cl—+Br2 |
| B.b处溶液显蓝色:2I—+Cl2=2Cl—+I2 |
| C.c出溶液的红色褪去:2OH—+Cl2=Cl—+ClO—+H2O |
| D.d处溶液显红色:Fe2++Cl2=Fe3++2Cl— |
下列反应必须加入氧化剂且一步反应就能完成的是
①KClO3→O2 ②Cl2→HCl ③HNO3→O2 ④N2→NO ⑤N2→NH3
| A.④ | B.②⑤ | C.①③ | D.①②③④ |
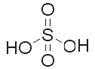
氨基磺酸(又叫固体硫酸)是重要的精细化工产品,广泛应用于金属和陶瓷制造的多种工业设备和民用设备清洗剂。下列有关的说法正确的是
| 氨基磺酸 |
硫酸 |
 |
 |
A.氨基磺酸的摩尔质量为97
B.SO2能用浓硫酸干燥,是因为SO2无还原性
C.氨基磺酸水溶液加热后生成NH4HSO4
D.13g锌与足量的其水溶液反应,生成4.48L H2
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可采取多种分类方法.表中各组归类中不合理的是
| 选项 |
按某一分类标准分类的一组 |
归类 |
| A |
FeSO4、NO2 、MnO2、NaClO |
H2SO3 |
| B |
CH3COOH、HClO、H2S、HOOC-COOH |
HF |
| C |
加聚反应、离子反应、放热反应、氧化还原反应 |
焰色反应 |
| D |
(NH4)2SO4、NH4Cl、NH4NO3、NH3•H2O |
NH4HCO3 |
9月2日中午,烧烤店服务员违规添酒精导致女大学生严重烧伤。下列说法错误的是
| A.烧烤店采用电源替代酒精作为燃料是出于安全考虑 |
| B.酒精与水可以通过萃取到达分离的目的 |
| C.实验室燃着的酒精灯被碰倒着火,立即用湿毛巾盖灭 |
| D.酒精使蛋白体发生变性 |
下面有关电化学的图示,完全正确的是