下列过程都与热量变化有关,其中表述不正确的是:
| A.CO(g)的燃烧热是283.0 kJ/mol,则表示CO(g)燃烧反应的热化学方程式为 CO (g)+ 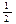 O2(g) O2(g) CO2 (g);△H=—283.0 kJ/mol CO2 (g);△H=—283.0 kJ/mol |
| B.稀盐酸和稀氢氧化钠溶液反应的中和热为57.3 kJ/mol,则表示稀硫酸与稀氢氧化钡溶液发生反应的热化学方程式为 1/2H2SO4(aq)+ 1/2Ba(OH)2(aq)=BaSO4(s)+H2O(l);△H=" —57.3" kJ/mol |
| C.铝热反应是放热反应,但需要足够的热量才能使反应发生 |
| D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O====4Al(OH)3,下列说法不正确的是( )
| A.正极反应式为:O2+2H2O+4e-====4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需更换铝板就可继续使用 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是()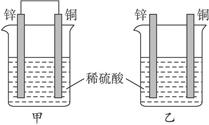
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 | D.产生气泡的速度甲比乙慢 |
某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4====Li2Mn2O4。下列说法正确的是()
| A.放电时,LiMn2O4发生氧化反应 |
| B.放电时,正极反应为:Li++LiMn2O4+e-====Li2Mn2O4 |
| C.充电时,LiMn2O4发生氧化反应 |
| D.充电时,阳极反应为:Li++e-====Li |
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时的电极反应式为
负极反应:C6Li-xe-====C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成的复合材料)
正极反应:Li1-xMO2+xLi++xe-====LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是()
| A.锂离子电池充电时电池反应为C6Li+Li1-x====MO2LiMO2+C6Li1-x |
| B.电池反应中,锂、锌、银、铅各失去1 mol电子,金属锂所消耗的质量最小 |
| C.锂离子电池放电时电池内部Li+向负极移动 |
| D.锂离子电池充电时阴极反应为C6Li1-x+xLi++xe-====C6Li |
下列说法正确的是()
| A.电解NaOH溶液时,溶液浓度将减小,pH增大 |
| B.电解H2SO4溶液时,溶液浓度将增大,pH减小 |
| C.电解Na2SO4溶液时,溶液浓度将增大,pH不变 |
| D.电解NaCl溶液时,溶液浓度将减小,pH不变 |