.2006年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是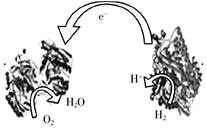
| A.左边为该电池的负极 |
| B.该电池可在高温环境下使用 |
| C.该电池负极反应为:H2—2e-=2H+ |
| D.该电 池正极反应为O2+4e-=2O2- |
某元素的电离能(单位:电子伏特)如下表,此元素位于元素周期表的族数是()
| I1 |
I2 |
I3 |
I4 |
I5 |
I6 |
I7 |
| 14.5 |
29.6 |
47.4 |
77.5 |
97.9 |
551.9 |
666.8 |
A. ⅢA B.ⅣAC.ⅥAD.ⅤA
下列事实与氢键有关的是()
| A.水加热到很高的温度都难以分解 |
| B.水结成冰体积膨胀 |
| C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |
下列各选项所述的两个量,前者一定大于后者的是()
①Al原子和N原子的未成对电子数;②Ag+、Cu2+与NH3形成配合物时的配位数;③Al的金属性和Mg的金属性;④F元素和O元素的电负性;⑤N和O元素的第一电离能;⑥H 原子和H+离子的半径
| A.①④⑤ | B.②④⑥ | C.④⑤⑥ | D.③⑤⑥ |
下列叙述正确的是 ( )
| A.分子晶体中的每个分子内一定含有极性共价键 |
| B.原子晶体中的相邻原子间只存在非极性共价键 |
| C.含有阴离子的化合物一定含有阳离子 |
| D.金属晶体的熔点和沸点都很高 |
下列粒子半径之比大于1的是
| A.K+/K | B.Mg / Ca | C.O2- / Na+ | D.Cl / Cl- |