用下列实验装置进行的实验,能达到相应的实验目的的是( )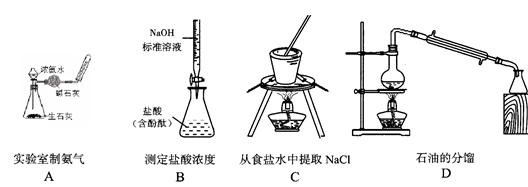
甲、乙两烧杯中分别装有相同体积、相同pH的氨水和NaOH溶液,各加入10mL 0.1 mol·L-1 AlCl3溶液,两烧杯中都有沉淀生成。下列判断正确的是()
| A.甲中沉淀一定比乙中的多 | B.甲中沉淀可能比乙中的多 |
| C.甲中沉淀一定比乙中的少 | D.实验过程中甲中和乙中的现象始终保持一致 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.25℃时,PH=13的1.0L Ba(OH)2溶液中含有的OH-离子数目为0.2NA |
| B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.标准状况下,22.4L SO3中含有的氧原子数为3.0NA |
下列实验操作或原理不正确的是( )
| A.除去氯化钠晶体中少量的硝酸钾 |
| B.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| C.只用淀粉溶液即可检验加碘食盐中是否含碘酸盐,从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
| D.可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油 |
下列除杂质的方法不可行的是( )
| A.用过量氨水除去Al3+溶液中的少量Cu2+ |
| B.将混合气体通过灼热的铜网除去N2中的少量O2 |
| C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D.用盐酸除去AgCl中少量的Ag2CO3 |