I.某校化学实验小组探究浓度对化学反应速率的影响,并测定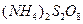 和KI反应的化学反应速率。进行如下实验探究:
和KI反应的化学反应速率。进行如下实验探究:
【实验原理】
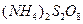 和KI反应的离子方程式为:
和KI反应的离子方程式为:
 (1)
(1)
平均反应速率的计算式为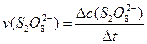 。
。
实验时,向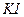 、
、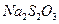 和淀粉指示剂混合溶液中加入
和淀粉指示剂混合溶液中加入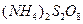 溶液,不断搅拌。在反应(1)进行的同时,发生反应:
溶液,不断搅拌。在反应(1)进行的同时,发生反应:
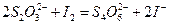 (2)
(2)
反应(1)生成的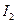 立即与
立即与 反应,生成无色的
反应,生成无色的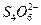 和
和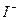 。
。 耗尽时,反应(1)继续生成的
耗尽时,反应(1)继续生成的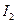 才与淀粉作用呈现蓝色。从加入
才与淀粉作用呈现蓝色。从加入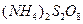 溶液到出现蓝色的时间为
溶液到出现蓝色的时间为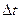 。
。
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
|
| 试剂 用量 (mL) |
0.20 mol·L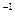 (NH4)2S2O8溶液 (NH4)2S2O8溶液 |
20.0 |
10.0 |
b |
20.0 |
20.0 |
0.20 mol·L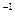 KI溶液 KI溶液 |
20.0 |
20.0 |
20.0 |
10.0 |
5.0 |
|
0.010 mol·L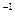 Na2S2O3溶液 Na2S2O3溶液 |
a |
8.0 |
8.0 |
8.0 |
8.0 |
|
| 0.2%淀粉溶液 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
|
0.20 mol·L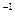 KNO3溶液 KNO3溶液 |
0 |
0 |
0 |
10.0 |
c |
|
0.20 mol·L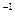 (NH4)2SO4溶液 (NH4)2SO4溶液 |
0 |
10.0 |
15.0 |
0 |
0 |
|
20℃时,反应时间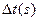 |
32 |
67 |
130 |
66 |
135 |
|
| 为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 |
||||||
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是 。
(3)第①组实验的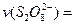 mol·(L·s)
mol·(L·s)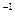 。
。
(4)根据上表数据分析,可以得到的结论有(写出一条即可) 。
II.实验小组查资料得知,向含有NaCO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:
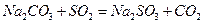

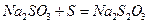
该小组根据上述原理设计如图19所示装置制备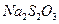 。
。
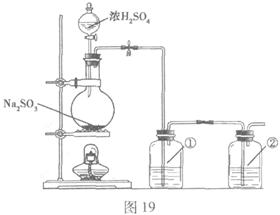
(1)实验应避免有害气体排放到空气中。装置①、②中盛放的试剂依次是① ;
② 。
(2)实验过程中,随着气体的通入,装置①中有大量黄色固体析出,继续通入气体,可以观察到的现象是 。
(3)反应结束后,从制得的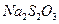 稀溶液中得到
稀溶液中得到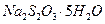 晶体的主要操作包括: 。
晶体的主要操作包括: 。
X、Y、Z、W均为含有10电子的微粒,W为金属阳离子,X、Y、Z常温下为气体,
(1)已知: W + X + H2O → 白色沉淀。
①若实验室用下图所示装置、干燥和收集装置制取并收集干燥的X,A中分液漏斗中的液态试剂的仪器的名称是________,仪器的连接顺序为a→________________________;
②由W离子形成的可溶性盐WCln,其水溶液显_________性,原因是(用离子方程式表示)_____________________________________________________
③为进一步确定W,进行如下实验,请补全实验操作、现象和结论:取上述白色沉淀少量置于试管中,_____________________________________________________
(2)常温下,取10 mLpH= a的Y的稀溶液,加水稀释时pH随溶液体积V的变化如图所示,则①Y的化学式为__________。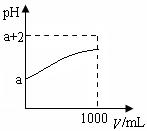
②下列有关Y的叙述正确的是__________
| A.Y溶于水后部分发生电离 |
| B.Y的水溶液中滴加石蕊试液会变红 |
| C.稀释后溶液中所有离子的浓度均减小 |
| D.稀释后,阴离子的物质的量浓度之和不变 |
③一定量X溶液和一定量的Y的溶液混合,所得溶液中离子浓度的等式关系为:
(用实际离子符号表示)
(3)已知H2的燃烧热为285.8 kJ·mol-1。现有Z和H2的混合气体共0.2 mol,与O2完全燃烧生成H2O(l)和CO2(g),转移电子的物质的量为1.0 mol,放出的热量为117.6 kJ。写出Z完全燃烧的热化学反应方程式__________________________________
2008年9月以来,三聚氰胺成为人们谈论的焦点。某同学为了测定三聚氰胺的分子式和结构简式。设计了如下实验。他查阅资料得知:三聚氰胺的相对分子质量为126,三聚氰胺在常温下为晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水。现有12.6g三聚氰胺晶体按下图所示实验装置反应(假设三聚氰胺完全转化成产物)。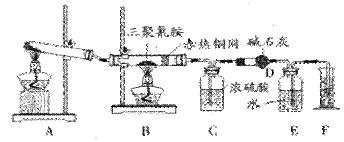
(1)写出A装置中发生反应的化学方程式:______________________________ ________
(2)C装置能不能与D装置互换?(填“能”或“不能”),理由是___________,___
_。
(3)当B装置中反应完全发生后,读取F中水的体积,实验操作顺序为__________(填序号)。
①读数②冷却至室温③调平E、F装置中液面
(4)测定数据如下:
经测定,收集到的气体折合成标准状况下的体积为6.72L。
①利用上述实验数据,通过计算可知三聚氰胺的实验式为_____________。
②三聚氰胺的分子式为_____________________。
③若装置中没有铜网,则对测定结果的影响是_____________________。
(5)已知氰酸(HCN)的结构简式为H—C≡N,氰胺的结构简式为H2N一C≡N,三聚氰胺分子中每个原子的最外层电子数均为8或2,则其结构简式为
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式,并指出其反应类型:_____ _________ ,属于_______________反应。
(2)浓硫酸的作用是:①_________________________;②____________________。
(3)装置中通蒸气的导管要插在_____________溶液的液面上,不能插入溶液中,目的是防止_______ 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是___________。
A.蒸馏 B.分液 C.过滤 D.结晶
(5)用30克乙酸与46克乙醇反应,如果实际产率是理论产率的67%,则可得到乙酸乙酯的质量是______________。
A.29.5克 B.44克 C.74.8克 D.88克
三位同学为了探究Na2CO3与CuSO4反应产生蓝色沉淀的成分,将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。甲同学认为:两者反应生成只有CuCO3一种沉淀;乙同学认为:这两者相互促进水解反应,生成Cu(OH)2一种沉淀;丙同学认为:生成CuCO3和Cu(OH)2两种沉淀(CuCO3和Cu(OH)2均不带结晶水)。
Ⅰ.按照乙同学的理解反应的化学反应方程式为:;
Ⅱ.在探究沉淀物成分前,须将沉淀从溶液中分离并净化。请用下图所示装置,选择必要的试剂,定性探究生成物的成分。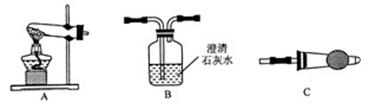
(1)装置C中装有试剂的名称是。
(2)能证明甲同学观点正确的实验现象是,能证明乙同学观点正确的实验现象是。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。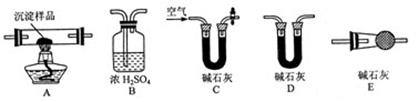
(3)各装置连接顺序为→→→→。
(4)装置C中碱石灰的作用是,实验开始时和实验结束时都要通入过量且处理过的空气其作用都是。
(5)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为。
(10分) 二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂,常温下二氧化氯为黄绿色或橘黄色气体,易溶于水,易与碱液反应,其性质非常不稳定,温度过高、二氧化氯的水溶液质量分数高于30%等均有可能引起爆炸。某研究小组设计下图所示实验装置制备ClO2。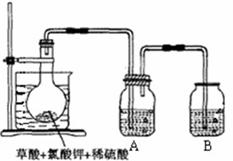
现称取12.25gKClO3和9g草酸(H2C2O4)放入烧瓶中,然后再加入足量的稀硫酸,水浴加热。
回答下列问题:
(1)已知反应后的产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为。
(2)在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其保持在60℃~
80℃之间。这样操作的目的是,
图示装置中缺少的一种必须的玻璃仪器是。
(3)A装置用于吸收产生的二氧化氯,其中最好盛放(填序号)。
a. 50mL 60℃的温水 b. 50mL冰水 c. 50mL饱和食盐水 d. 50mL NaOH溶液
(4)本实验所制得的二氧化氯水溶液质量分数约为。(小数点后保留两位)
(5)二氧化氯可迅速氧化硫化物,以除去有机硫产生的臭味,改善水产养殖水体的水质。取适量二氧化氯溶液加入到硫化氢溶液中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。硫化氢溶液与二氧化氯发生反应的离子方程式为。