为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
| 实验序号 |
样品的质量/g |
NaOH溶液的体积/mL |
氨气的体积/L |
| Ⅰ |
7.4 |
40.00 |
1.68 |
| Ⅱ |
14.8 |
40.00 |
3.36 |
| Ⅲ |
22.2 |
40.00 |
1.12 |
| Ⅳ |
37.0 |
40.00 |
0 |
(1) 测定过程中有关反应的离子方程式为
______________________________ 。
(2) 3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为__________L。
(3) 试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4) 欲计算该NaOH溶液的物质的量浓度应选择第______组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程。
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++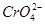 ,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(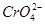 )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
(1)Cl-、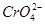 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是多少?(设混合溶液在反应中体积不变)
铬酸银在298 K时的溶解度为0.004 45 g,求其溶度积。
取1.43g Na2CO3·xH2O 溶于水配成10mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0m L,并收集到112m LCO2(标准状况)。
求(1)稀盐酸物质的量浓度(2)Na2CO3·XH2O 的摩尔质量(3)x值
把19.2 g 的Cu放入500mL 2 mol∙L−1稀硝酸中,充分反应,Cu完全溶解。求:
(1)写出Cu与稀硝酸反应的离子方程式:;
(2)转移电子数目为(用含NA的式子表示);
(3)氧化剂与还原剂的物质的量比为。
(4)反应后溶液中C(H+)为(体积变化忽略不计)
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的氢气时,硫酸恰好用完,则:
(1)产生这些气体消耗的锌的质 量是多少?
(2)通过导线的电子的物质的量是多少?
(3)原稀硫酸的物质的量浓度是多少?