现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算pH时假定溶液体积没有变化):
①向其中一份固体中加入100mL 2.0mol·L-1的NaOH溶液,加热使其充分反应后过滤,测得滤液的pH=14;
②向另一份固体中加入100mL 4.0 mol·L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且 pH=1。
pH=1。
则②产生气体的体积(标准状况)为( )
| A.2.352L | B.2.448L | C.2.688L | D.2.856L |
下列有机物是 的同系物的是 ()
的同系物的是 ()
A. |
B.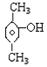 |
C.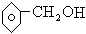 |
D. |
C2H5OH和C3H6OH组成的混合物在一定条件下发生脱水反应(包括分子内脱水和分子间脱水)最多生成有机物有多少种()
| A.5种 | B.6种 | C.8种 | D.9种 |
生活中碰到的某些问题常常涉及到化学知识,下列叙述正确的是()
①人的皮肤在强紫外线的照射下将会失去生理活性
②为了防止海产食品腐烂变质,用甲醛溶液浸泡
③油脂变质会发出难闻的特殊气味,是由油脂的物理性质决定的
④蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
⑤四氯化碳和苯是常见的有机溶剂,日常用于清洗衣服上的油污
| A.①④ | B.②③④ | C.①②④⑤ | D.全部 |
一定条件下,下列物质可跟下图所示有机物反应的是()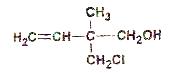
(1)酸性KMnO4溶液 (2)NaOH溶液 (3)KOH醇溶液
(4)Na (5)CuO
| A.(1)(2)(4) | B.(1)(3)(4) |
| C.(1)(2)(4)(5) | D.全部 |
糖类、脂肪和蛋白质是维持人体生命活动所必需三大营养物质。以下叙述正确的是()
| A.植物油不能使溴的四氯化碳溶液褪色 |
| B.淀粉水解的最终产物是葡萄糖 |
| C.葡萄糖能发生氧化反应和水解反应 |
| D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |