工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但钾却不能用电解熔融KCl的方法制得,因金属钾易溶于熔融态的KCl中而有危险,难获得钾,且降低电流效率。现生产钾是用属钠和熔化的KCl在一定的条件下反应制取:
有关数据如下表:
| |
熔点℃ |
沸点℃ |
密度(g/cm3) |
| Na |
97.8 |
882.9 |
0.97 |
| K |
63.7 |
774 |
0.86 |
| NaCl |
801 |
1413 |
2.165 |
| KCl |
770 |
1500(升华) |
1.984 |
(1)工业上制取金属钾的化学原理是 ,在常压下金属钾转为气态从反应混合物中分离的最低温度约为 ,而反应的最高温度应低于 。
(2)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是 。
(3)生产中常向反应物中通入一种气体,并将从反应器中导出的气体进行冷却得到金属钾,且将该气体可循环利用,该气体是________。
a.干燥的空气 b.氮气 c.二氧化碳 d.稀有气体
(4)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为K= 。
汞单质及其化合物在工业生产和科学实验中有广泛的用途,汞的矿源是朱砂(HgS)。朱砂炼汞的反应之一为(在加热条件下进行):HgS + O2 =" Hg" + SO2
请回答:
HgS与O2的反应中,氧化剂是,每生成1molHg转移电子的物质的量为
中学化学中几种常见物质的转化关系如下图(有部分产物未画出)。A是一种金属单质,D是一种非金属固体单质。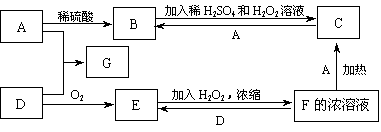
回答下列问题:
(1)A是 G是
(2)请写出鉴定B中阳离子的实验方法和现象
(3)在酸性条件下,再举出可使B转化为C的两种试剂
(4)写出反应C+A→B的离子方程式:
(5)写出反应E+H2O2→F的化学方程式:
X、Y、Z、E和F分别代表原子序数依次增大的五种短周期元素,它们满足以下条件:①Z元素的原子半径是短周期元素中除稀有气体外半径最大的;②X与Z同主族,Y与F同主族;③X与F可组成化学式为X2F的共价化合物;④Z和E二者的最高价氧化物对应的水化物之间能发生反应。请填空:
(1)写出F元素在元素周期表中的位置
(2)X和Y可形成电子数相等的两种粒子,该两 种粒子反应后生成一种中性分子,反应的离子方程式是。
种粒子反应后生成一种中性分子,反应的离子方程式是。
(3)写出单质E与Z的最高价氧化物的水化物反应的离子方程式:。
(4)均含有X、Y、Z和F四种元素的两种化合物在溶液中发生反应的离子方程式
。
已知:两个羟基同时连在同一碳原子上的结构是不稳定的,它将发生脱水反应CH3CH(OH)2 CH3CHO+H2O现有分子式为C9H8O2Br2的物质M,已知有机物C的相对分子质量为60,E的化学式为C7H5O2Na在一定条件下可发生下述一系列反应:
CH3CHO+H2O现有分子式为C9H8O2Br2的物质M,已知有机物C的相对分子质量为60,E的化学式为C7H5O2Na在一定条件下可发生下述一系列反应:
请回答下列问题:
(1)B中官能名称是,A的核磁共振氢谱图有个吸收峰。
(2)M的结构简式为 _________;C的结构简式为 __________。
(3 )G→H的反应类型是 ____
)G→H的反应类型是 ____ __;H→I的反应类型是 ______;
__;H→I的反应类型是 ______;
(4)写出下列反应的化学方程式:
①E→ F的化学方程式: _______ ;
;
②H→I的化学方程式: ___。
(5)请写出同时符合下列条件的G的同分异构体的结构简式。(任写一种)a.分子中含有苯环 b.能发生水解反应
c.能发生银镜反应 d.与FeCl3溶液反应显紫色
现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
OH-、Cl-、NO3-、CO32-、SO42- |
已知:
① A、B两溶液呈碱性,C、D、E溶液呈酸性。
常温下,0.1mol/L A溶液的pH小于13,
0.1mol/L C溶液的pH小于1。
②A溶液与E溶液反应既有气体又有 沉淀产生;
沉淀产生;
A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)写出D的化学式:。
(2)将E溶液加热蒸干并灼烧所得产物的名称为:;
(3)写出A、E溶液反应的离子方程式:;
(4)写出B溶液与C溶液恰好完全反应至溶液呈中性的离子方程式: