氯化亚铜(CuCl)是重要的化工原料。工业上常通过下列反应制备CuCl:
2CuSO4+Na2SO3+2NaCl+Na2CO3→2CuCl↓+3Na2SO4+CO2↑
(1)CuCl制备过程中需要配制质量分数为20.0%的CuSO4溶液,配制该溶液所需的CuSO4·5H2O与H2O的质量之比为 。
(2)准确称取所配制的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1的Ce(SO4)2溶液滴定到终点,消耗24.60mLCe(SO4)2溶液。有关反应的离子方程式为:
Fe3++CuCl→Fe2++Cu2++Cl- Ce4++Fe2+→Fe3++Ce3+
已知国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.50%。试通过计算说明上述样品中CuCl的质量分数是否符合国家标准。
用15.8g KMnO4氧化75mL足量浓盐酸。反应方程式如下:
2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑+ 8H2O
(1)有多少克HCl被氧化?
(2)若向反应后的剩余溶液中,加入足量AgNO3溶液,生成沉淀57.4g,求原浓盐酸的物质的量浓度?
取一定量的Na2CO3、NaHCO3和Na2SO4混合物与250mL 1.00mol·L-1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100mol·L-1Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL 1.00mol·L-1盐酸恰好完全中和。计算混合物中各物质的质量。
95℃时水的离子积为1×10-12,在该温度下将pH=8的Ba(OH)2溶液与PH=4的稀硫酸溶液混合,欲使混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为多少?(假设二者混合后的体积为二者体积之和)
如图所示,离地面足够高处有一竖直的空管,质量为2kg,管长为24m,M、N为空管的上、下两端,空管受到F=16N竖直向上的拉力作用,由静止开始竖直向下做加速运动,同时在M处一个大小不计的小球沿管的轴线以初速度v0竖直上抛,不计一切阻力,取g=10m/s2.求:
(1)若小球上抛的初速度为10m/s,经过多长时间从管的N端穿出?
(2)若此空管的N端距离地面64m高,欲使在空管到达地面时小球必须落到管内,在其他条件不变的前提下,求小球的初速度v0大小的范围.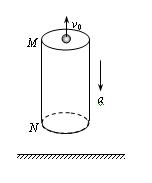
如图为宇宙中有一个恒星系的示意图。A为星系的一颗行星,它绕中央恒星O运行的轨道近似为圆。天文学家观测得到A行星运动的轨道半径为 、周期为
、周期为 。
。
(1)中央恒星O的质量为多大?
(2)经长期观测发现,A行星实际运动的轨道与圆轨道总存在一些偏离,且周期性地每隔时间 发生一次最大的偏离。天文学家认为形成这种现象的原因可能是A行星外侧还存在着一颗未知的行星B(假设其运行轨道与A在同一水平面内,且与A的绕行方向相同),它对A行星的万有引力引起A轨道的偏离。(由于B对A的吸引而使A的周期引起的变化可以忽略)根据上述现象及假设,试求未知行星B的运动周期T及轨道半径R。
发生一次最大的偏离。天文学家认为形成这种现象的原因可能是A行星外侧还存在着一颗未知的行星B(假设其运行轨道与A在同一水平面内,且与A的绕行方向相同),它对A行星的万有引力引起A轨道的偏离。(由于B对A的吸引而使A的周期引起的变化可以忽略)根据上述现象及假设,试求未知行星B的运动周期T及轨道半径R。