元素X、Y、Z原子序数之和为37,X、Y在同一周期,X+与Z-具有相同的核外电子层结构。下列推测不正确的是
| A.同周期元素中X的金属性最强 | B.原子半径X>Y,离子半径X+>Z- |
| C.同族元素中Z的氢化物稳定性最高 | D.同周期元素中Y的最高价含氧酸的酸性最强 |
某含氧酸的化学式为Hn RO2n+2,试判断R的最合理价态为()
RO2n+2,试判断R的最合理价态为()
| A.+7 | B.+6 | C.+5 | D.+4 |
下列各项所述的数字不是6的是( )
| A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl- 的个数 |
| B.在金刚石晶体中,最小的环上的碳原子个数 |
| C.在二氧化硅晶体中,最小的环上的原子个数 |
| D.在石墨晶体的片层结构中,最小的环上的碳原子个数 |
已知单质碘微溶于水,易溶于碘化钾溶液,下列对碘单质易溶于碘化钾水溶液的原因分析正确的是
| A.KI属于共价化合物,与I2分子相似相溶 |
| B.I2是离子化合物,与KI相似相溶 |
| C.KI与I2发生化学反应生成的新化合物具有强极性,与H2O相似相溶 |
| D.在KI与I2中均含有碘元素,含有同种元素的物质相似相溶 |
据报道,某种合金材料有较大的储氢容量,其晶体结构的最小单元如右图所示。则这种合金的化学式为()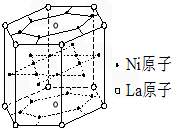
| A.LaNi6 | B.LaNi3 | C.LaNi4 | D.LaNi5 |
最近,中国科大的科学家们将C60分子组装在一单层分子膜表面,在—268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图像。下列化合 物分子中一定既含单键又含双键的是( )
物分子中一定既含单键又含双键的是( )
| A.COCl2 | B.C2H4O | C.CO2 | D.H2O2 |