某种酯的结构可表示为:CmH2m+1COOCnH2n+1,其中m+n=5,该酯的一种水解产物经催化氧化可转化成它的另一种水解产物,则原来的酯是
| A.丙酸乙酯 | B.乙酸乙酯 | C.丁酸甲酯 | D.丙酸丙酯 |
已知HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是
| A.对比等浓度的两种酸溶液的pH |
| B.对比等浓度的两种酸溶液,与相同大小镁条反应的初始速率 |
| C.对比等浓度、等体积的两种酸溶液,与等量NaOH溶液反应后放出的热量 |
| D.对比等浓度、等体积的两种酸溶液,与足量Zn反应,生成H2的体积 |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+) / c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是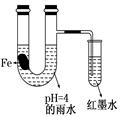
| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C.墨水液面回升时,正极反应式为:O2+2H2O+4e—==4OH- |
| D.U型管中溶液pH逐渐减小 |
某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能)。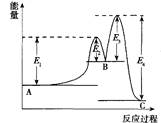
下列有关叙述正确的是
| A.两步反应均为吸热反应 |
| B.加入催化剂会改变反应的焓变 |
| C.三种化合物中C最稳定 |
| D.A→C反应中ΔH = E1 - E2 |
将左下图中所示实验装置的K闭合,下列判断正确的是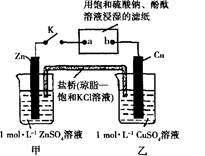
| A.电子沿Zn→a→b→Cu路径流动 |
| B.Cu电极质量增加 |
| C.甲池与乙池中的溶液互换,闭合K,电流没有明显变化 |
| D.片刻后可观察到滤纸b点变红色 |