下列溶液中各微粒的浓度关系正确的是
A.0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1
B.0.1 mol/L NaHCO3溶液中,c(Na+) = 2c(CO32—) + c(HCO3—) + c(H2CO3)
C.0.1 mol/L 的NaHA溶液,其pH = 4,则c(HA—)>c(A2—)>c(H2A)
D.只含Na+、CH3COO—、H+、OH—的酸性溶液中,c(H+)>c(CH3COO—)>c(Na+)>c(OH—)
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)。
下列有关说法不正确的是
| A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程 |
| B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| C.在过程③⑤中溴元素均被氧化 |
D.过程①中除去粗盐中的SO 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
设NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.25℃,pH=2的HCl溶液中含有H+的数目为0.01NA |
| B.1mol Na2O2固体中含有的阴阳离子总数为4 NA |
| C.1mol碳烯(:CH2)中含有的电子数8NA |
| D.5.6g铁粉与硝酸反应失去的电子数一定为0.3 NA |
已知101kPa下有:H2(g)+1/2 O2(g)=H2O(g);△H=-241.8kJ/mol。则下列说法或表达中正确的是()
| A.H2的燃烧热为241.8kJ/mol |
| B.H2(g)+1/2O2(g)=H2O(l);△H<-241.8kJ/mol |
| C.2H2(g)+O2(g)=2H2O(g);△H>-241.8kJ/mol |
| D.1molH2与1/2molO2的总能量小于1molH2O(g)的总能量 |
下列离子方程式表示正确的是
| A.AgNO3溶液中加入Cu :Cu+Ag+=Cu2++Ag |
| B.NaHCO3溶液中加入CH3COOH:CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O |
| C.0.1mol FeBr2溶液中通入足量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| D.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
某同学如图所示装置进行实验,当滴入液体后出现气球体积缩小了,则使用的固体和液体试剂可能是()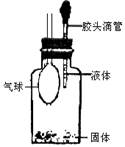
| A.铜与浓硫酸 | B.铁与浓硫酸 |
| C.铝和氢氧化钠溶液 | D.二氧化锰和浓盐酸 |