把铝粉与Fe3O4的混合物,分为两等份。前一份在高温下恰好完全反应,之后将生成物与足量盐酸充分反应;后一份直接加入足量NaOH溶液充分反应。前后两种情况下生成的气体在同温同压下的体积比是
| A.1:1 | B.3:4 | C.9:8 | D.4:3 |
在已达到电离平衡的0.1 mol·L-1的醋酸溶液中,欲使平衡向电离的方向移动,同时使溶液的pH 降低,应采取的措施是
| A.加少量水 | B.加热 |
| C.加少量盐酸 | D.加少量醋酸钠晶体 |
对于3Fe(s)+4H2O(g)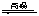 Fe3O4(s)+4H2(g),化学平衡常数的表达式为
Fe3O4(s)+4H2(g),化学平衡常数的表达式为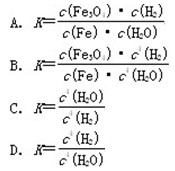
在体积可变的密闭容器中,反应mA(g)+nB(s) pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低,下列说法中,正确的是
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低,下列说法中,正确的是
| A.(m+n)必定小于p | B.(m+n)必定大于p |
| C.m必定小于p | D.m必定大于p |
NO2中存在下列平衡:2NO2 N2O4(g)(正反应是放热反应)。在测定NO2的相对分子质量时,下列条件中较为适宜的是
N2O4(g)(正反应是放热反应)。在测定NO2的相对分子质量时,下列条件中较为适宜的是
| A.温度130 ℃,压强3.03×105 Pa |
| B.温度25 ℃,压强1.01×105 Pa |
| C.温度130 ℃,压强5.05×104 Pa |
| D.温度0 ℃,压强5.05×104 Pa |
在一定温度下,可逆反应A(g) + 3B(g) 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A、C生成的速率和C分解的速率相等
B、A、B、C的浓度相等
C、单位时间内生成n摩A,同时生成3n摩B
D、A、B、C的分子数之比为1:3:2