“甲型H1N1”流感疫情已构成“具有国际影响的公共卫生紧急事态”。已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性。其分子结构如右图:下列说法正确的是
| A.该物质的分子式为C12H19N4O7 |
| B.在一定条件下,该物质可以发生消去、加成、取代等反应 |
| C.1mol该物质与NaOH溶液反应,可以消耗4mol NaOH |
| D.该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色应 |
实验室制Cl2时有如下操作,其顺序正确的是( )
①连接好装置,检查气密性②缓缓加热③加入MnO2粉末④用分液漏斗向烧杯中加盐酸⑤将多余Cl2通入NaOH溶液中⑥用向上排空气法收集Cl2
| A.①②③④⑤⑥ | B.①③④②⑥⑤ |
| C.③④②①⑥⑤ | D.①③④②⑤⑥ |
除去Cl2中混有的水蒸气和氯化氢气体,可使气体依次通过盛有下列物质的洗气瓶( )
| A.浓硫酸、水 | B.饱和食盐水、浓H2SO4 |
| C.烧碱、石灰水 | D.无水CaCl2、烧碱 |
下列物质能使红墨水褪色的是( )
| A.活性炭 | B.CO2 | C.NaCl溶液 | D.酸化的NaClO溶液 |
已知KMnO4与浓盐酸在常温下反应能生成Cl2。若用图4-7所示的实验装置来制备纯净、干燥的氯气,并实验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是()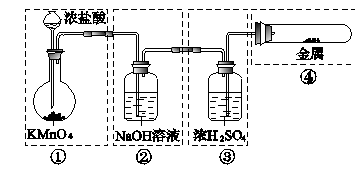
图4-7
| A.①和②处 | B.②处 | C.②和③处 | D.②③④处 |
密闭容器中盛有氢气和氯气的混合气体,用电火花引爆后恢复到原状况,用足量NaOH溶液吸收后无气体剩余,原混合气体中氯气与氢气的体积比可能是()
| A.>1∶1 | B.=1∶1 | C.<1∶1 | D.无法确定 |