下列离子方程式正确的是( )
A乙酸与碳酸钠溶液反应:2H++CO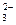 == CO2↑+H2O
== CO2↑+H2O
B醋酸溶液与新制氢氧化铜反应:
CH3COOH+OH-—→ CH3COO-+H2O
C苯酚钠溶液中通入少量二氧化碳:
2C6H5O-+CO2+H2O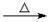 2C6H5OH+CO
2C6H5OH+CO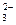
D甲醛溶液与足量的银氨溶液共热
HCHO+4[Ag(NH3)2]++4OH-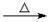 CO
CO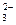 +2NH
+2NH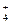 +4Ag↓+6NH3+2H2O
+4Ag↓+6NH3+2H2O
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是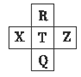
| A.元素R对应气态氢化物的相对分子质量实际测量值往往比理论上要大的多,这可能和氢键有关 |
| B.由于键能E(H-R)>E(H-T),故元素R、T对应气态氢化物的沸点:HR>HT |
| C.R与Q的电子数相差16 |
| D.最高价氧化物对应的水化物的酸性:X<T<Q |
下列说法正确的是
| A.用电子天平称量化学药品时,必须先称小烧杯的质量,再称量加入试剂后的总质量,两者之差即为药品的质量 |
| B.配制100mL 0.25mol·L-1的NaOH溶液必须用到的仪器有:100mL容量瓶、托盘天平或电子天平、烧杯、玻璃棒、量简或移液管、胶头滴管 |
| C.向K2Cr2O7酸性溶液滴入NaNO2溶液,溶液由橙色变成黄色,体现了NO2-的氧化性 |
| D.可以用碳酸钠溶液将乙酸、乙醇和乙酸乙醋鉴别开来 |
下列说法不正确的是
| A.中国是目前全球最大的稀土提炼和加工国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 |
| B.气化、液化和干馏是煤综合利用的主要方法,这三者中只有干馏是化学变化 |
| C.一些有机溶剂(如乙醚、乙醇、苯、丙酮等)沸点低极易被引燃,加热时最好用水浴加热 |
| D.分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
下列说法正确的是
| A.已知CO(g)的燃烧热ΔH=-283.0 kJ·mol-1,则表示CO燃烧热的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ/mol |
| B.等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多。 |
C.在稀溶液中, ,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ ,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D.由N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ·mol-1,可知将1 mol N2(g)和3 mol H2(g)置于密闭容器中充分反应后放出热量为92.4 kJ |
N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是
| A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+="=" 2NH4+ |
| B.反应过程中溶液的pH会变大,故需要加入盐酸 |
| C.该电池外电路电流从通入H2的电极流向通入N2的电极 |
| D.通入H2的电极为负极,A为NH4Cl |