下列化合物中既有离子键又有共价键和配位键的是()
| A.KF | B.H2SO4 | C.CuCl2 | D.NH4Cl |
下列叙述不正确的是()
| A.Na、Mg、Al的第一电离能依次减弱 |
| B.H2S、H2O、HF的稳定性依次增强 |
| C.NaOH、Mg(OH)2、Al(OH)3的碱性依次减弱 |
| D.H4SiO4、H2CO3、H2SO4酸性依次增强 |
下列各原子或离子的电子排列式错误的是()
| A.Na+ 1s22s22p6 | B.N3-1s22s22p3 | C.F¯ 1s22s22p6 | D.O 1s22s22p4 |
下列含有极性键的非极性分子是()
(1)CCl4(2)NH3(3)CH4(4)CO2(5)N2
(6)H2S(7)SO2(8)CS2(9)H2O(10)HF
| A.(2)(3)(4)(5)(8) | B.(1)(3)(4)(5)(8) |
| C.(1)(3)(4)(8) | D.以上均不对 |
近年来,科学家合成了一系列具有独特化学特性的(AlH3)n氢铝化合物。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如图。下列有关说法肯定错误的是( )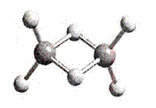
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |