设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.0.1mol·L-1氢氧化钠溶液中含钠离子数为0.1NA |
| B.7gCnH2n中含氢原子数为NA |
| C.1mol C5H12分子中共价键总数为13NA |
| D.标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA |
下图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是( )
| A.H2S | B.HCl | C.PH3 | D.SiH4 |
若ABn型分子的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是()
| A.若n=2,则分子的立体构型为V形 | B.若n=3,则分子的立体构型为三角锥形 |
| C.若n=4,则分子的立体构型为正四面体形 | D.以上说法都不正确 |
根据物质溶解性“相似相溶”的一般规律,能说明碘、溴单质在CCl4中比在水中溶解度大的是( )
| A.溴、碘单质和CCl4中都含有卤素 |
| B.溴、碘是单质,CCl4是化合物 |
| C.Cl2、Br2、I2是非极性分子,CCl4也是非极性分子,而水为极性分子 |
| D.以上说法都不对 |
某物质的实验式为PtCl4·2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
| A.配合物中中心原子的电荷数和配位数均为6 | B.该配合物可能是平面正方形结构 |
| C.Cl-和NH3分子均与Pt4+配位 | D.配合物中Cl-与Pt4+配位,而NH3分子不配位 |
以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是( )
| A.∶He | B.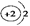 |
C.1s2 | D.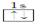 |