下列关于实验仪器和用品的选择,不正确的是
| A.实验室制备乙烯时加入碎瓷片,可以防止暴沸 |
| B.用KMnO4滴定H2C2O4时需要用到两支酸式滴定管 |
| C.进行中和热的测定实验时,必须用到两个量筒和两个温度计 |
| D.实验室测定化学反应速率时,需要用到仪器秒表 |
下列叙述正确的是
①7Li+中含有的中子数与电子数之比为2:1
②在C2H6分子中极性共价键与非极性共价键数之比为3:1
③常温下,11.2 L的甲烷气体中含有的氢、碳原子数之比为4:1
④5.6 g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2:1
| A.①② | B.②③ | C.①③ | D.③④ |
已知A、B为单质,C为化合物。
A+B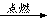 C
C
 A+B
A+B
能实现上述转化关系的是
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①②B.②④C.①③D.③④
元素周期表中同周期或同主族元素,随着原子序数的递增,下列说法正确的是
| A.ⅦA族元素的单质沸点逐渐降低 |
| B.ⅥA族元素的原子核外最外层电子数逐渐增多 |
| C.碱金属元素最高价氧化物的水化物碱性逐渐增强 |
| D.第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |
关于下列说法:①Fe(OH)3胶体和CuSO4溶液都是混合物;②BaSO4是一种难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④太阳能、氢能和海洋能都属于新能源;⑤置换反应都属于离子反应。其中正确的是
| A.①②④ | B.①②⑤ | C.②③④ | D.③④⑤ |
下列有关安全事故的处理不恰当的是
| A.不慎将苯酚沾到皮肤上,应立即用酒精洗涤 |
| B.一氧化碳中毒后,应尽快将中毒者抬到空气流通处 |
| C.不慎将浓硫酸沾到皮肤上,应立即用氢氧化钠溶液洗涤 |
| D.解救Cu2+、Hg2+等重金属盐中毒的病人,可让病人服用大量牛奶或豆浆 |