0.75 mol RO32-共有30 mol电子,则R在周期表中的位置是
| A.第二周期 | B.第四周期 | C.第ⅣA族 | D.第ⅥA族 |
醋酸是电解质,下列事实能说明醋酸是弱电解质的组合是()
①醋酸与水能以任意比互溶②醋酸溶液中存在醋酸分子
③醋酸能和碳酸钙反应放出CO2④0.1 mol·L-1醋酸钠溶液pH=8.9
⑤完全相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢
| A.①④⑤ | B.②③④ | C.②④⑤ | D.①③⑤ |
下列各溶液中,微粒的物质的量浓度关系正确的是()
| A.0.1mol·L-1 Na2CO3溶液:[OH—]=[HCO3—] + [H+] +[H2CO3] |
| B.0.1mol·L-1 NH4Cl溶液:[NH4+]=[Cl-] |
| C.向醋酸钠溶液中加入适量醋酸,得到酸性混合溶液:[Na+]>[CH3COO-]>[H+]>[OH-] |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液: [Na+]=[NO3-] |
常温下,把盐酸和氨水等体积混合后,其溶液的pH恰好等于7,则下列说法中正确的是()
| A.盐酸中的c(H+)一定小于氨水中的c(OH-) |
| B.盐酸的物质的量浓度一定小于氨水的物质的量浓度 |
| C.反应后生成的盐溶液一定没有发生水解 |
| D.盐酸中HCl的物质的量一定等于NH3・H2O的物质的量 |
在加入铝片有氢气产生的溶液中一定能够大量共存的离子组是()
| A.S2-、NO3-、Ba2+、Na+ | B.Na+、K+、SO42-、Cl- |
| C.NH4+、Ba2+、Cl-、HCO3- | D.SO42-、CH3COO-、Al3+、Mg2+ |
下列离子方程式正确的是()
A.碳酸钠溶于水中 CO32- + 2H2O 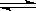 H2CO3 + 2OH- H2CO3 + 2OH- |
| B.氯化亚铁溶液中通入少量氯气 Fe2+ + Cl2= Fe3+ + 2Cl- |
| C.NH4HCO3溶液与过量NaOH稀溶液反应 NH4+ + OH-= NH3·H2O |
| D.少量Ba(OH)2溶液与NaHSO4溶液反应Ba2+ + 2OH- + 2H+ + SO42-= BaSO4↓+ 2H2O |