现有一瓶乙二醇和丙三醇的混和物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
| 物质 |
分子式 |
熔点℃ |
沸点℃ |
密度(g/cm3) |
溶解性 |
| 乙二醇 |
C2H6O2 |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
| 丙三醇 |
C3H8O3 |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
A 萃取法 B 结晶法 C 分液法 D 分馏法

短周期元素X、Y的原子序数相差2。下列有关叙述不正确的是()
| A.X与Y可能位于同一主族 |
| B.X与Y不一定位于同一周期 |
| C.X与Y可能形成离子化合物XY |
| D.X与Y不可能形成共价化合物XY |
磷酸氢二铵[(NH4)2HPO4]可用作复合肥料。关于该物质的下列说法不正确的是()
| A.HPO42-中含有共价键,其中P的化合价为+5价 |
B.是一种离子化合物,其中铵根离子的电子式为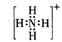 |
| C.该化合物中所有原子均满足8电子稳定结构 |
| D.其中P元素的质量分数比N元素的质量分数高 |
取四线湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加69%的硝酸、98.3%的硫酸、新制氯水、浓氨水,四张试纸最后呈现的颜色是()
| A.白、红、白、蓝 | B.白、黑、白、蓝 |
| C.白、白、白、蓝 | D.红、黑、红、蓝 |
在检验SO42-的过程中,下列操作中正确的是( )
| A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在 |
| B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在 |
| C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在 |
| D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在 |
下列实验用来证明SO2的存在,其中正确的是()
| A.能使品红褪色。 |
| B.能使湿润的蓝色石蕊试纸变红。 |
| C.通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸。 |
| D.通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸。 |