把mmol C2H4跟nmol H2 混合在密闭容器中,在适当条件下,反应达到平衡时生成pmolC2H6,若将所得平衡混和气体完全燃烧生成二氧化碳和水,需要氧气的量是
A (3m+n)mol B (3m+n/2)mol
C (3m+3p+n/2)mol D (3m+n/2-3p)mol
下列叙述正确的 ( )
| A.同一周期的非金属元素,由左到右其氧化物对应水化物的酸性依次递增 |
| B.aXn-与bYm+两种离子电子层结构相同,则b-a=n+m |
| C.同一主族非金属元素对应氢化物稳定性依次递增,是由于其相对分子质量依次递增、分子间作用力增强所导致的 |
| D.同一主族非金属元素对应氢化物沸点由上到下依次递增 |
核内中子数为N的R2+离子,质量数为A,则n克它的氧化物所含电子物质的量为( )
A.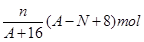 |
B. |
C.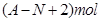 |
D. |
简单原子的原子结构可用下图的表示方法来形象表示,其中“黑球”表示质子或电子,“白球”表示中子。则下列有关①、②、③的叙述中正确的是( )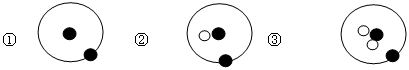
| A.①、②、③互为同位素 | B.①、②、③互为同素异形体 |
| C.①、②、③是三种化学性质不同的核素 | D.①、②、③质量数相同 |
以铁为阳极,以铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到2molFe(OH)3沉淀,此间共消耗的水的物质的量为
| A.2mol | B.3mol | C.4mol | D.5mol |
0.1 mol·L-1 AgNO3溶液在以Ag作阳极、Fe作阴极的电解槽中电解,当阴极上增重2.16 g时,下列判断正确的是
| A.溶液的浓度变为0.08 mol·L-1 | B.阳极上产生112 mL O2(标准状况) |
| C.转移的电子数是1.204×1023 | D.反应中有0.02 mol的Ag被氧化 |