某溶液中含有NH4+、SO32-、SiO42-、Br-、CO32-、Na+,向该溶液中通人过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+
②有胶状物质生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应
| A.①②③④ | B.②③④ | C.①③⑤ | D.②④⑤ |
【改编】十八大报告中提出“大力推进生态文明建设,提高生态文明水平,建设美丽中国”。化学已渗透到人类生活的各个方面。下列说法正确的是
| A.PM2.5是指大气中直径≤2.5厘米的颗粒物,只要戴普通口罩就对人体健康无影响 |
| B.绚丽缤纷的烟花中因为添加了含钾、钠、钙、铜等金属元素的化合物才显现出各种颜色 |
| C.明矾可以净水是因为明矾可以将水中的病毒氧化而达到消毒的目的 |
| D.维生素C又叫抗坏血酸,它具有很强的氧化性 |
【原创】下列说法正确的是
| A.乙酸是强酸 |
| B.甲烷、乙烯、苯都能发生加成反应 |
C.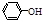 溶液显碱性 溶液显碱性 |
| D.CH3CH2OH + CH3COOH→CH3COOCH2CH3 + H2O这个反应是取代反应。 |
T ℃时,将6 mol CO2和8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
| A.反应开始至a点时v(H2)=1 mol·L-1·min-1 |
| B.若曲线Ⅰ对应的条件改变是升温,则该反应∆H>0 |
| C.曲线Ⅱ对应的条件改变是降低压强 |
| D.T ℃时,该反应的化学平衡常数为0.125 |
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是
| A.水既是氧化剂又是溶剂 | B.放电时正极上有氢气生成 |
| C.放电时OH﹣向正极移动 | D.总反应为:2Li+2H2O=2LiOH+H2↑ |
关于金属铝和铁的说法不正确的是
| A.铁与热水不反应,但是高温下可与水蒸气发生置换反应 |
| B.铝箔在空气中受热可以熔化,剧烈燃烧,产生大量的热 |
| C.常温下,可以用铝或铁制容器来盛装冷的浓硫酸或冷的浓硝酸 |
| D.铝元素是地壳中含量最多的金属元素,而铁是用途最广的金属 |