下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为 。
(2)⑥和⑦的最高价含氧酸的酸性强弱为 > 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
①写出D溶液与G反应的化学方程式 。
②写出检验A溶液中溶质的阴离子的方法 。
③常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为 mol。
④若上图中各步反应均为完全转化,则混合物x中含有的物质有 。
(1)相对分子质量为72的某烃,其一氯代物只有一种,则该烃的一氯代物的结构简式为______________________。
(2)某有机物含有C、H、O、N等四种元素,如上图为该有机物的球棍模型。该有机物的分子式为。结构简式为。
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有;
(2)硫酸铜溶液可以加快氢气生成速率的原因是;
(3)实验室中现有 、
、 、
、 、
、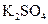 等4中溶液,可与实验中
等4中溶液,可与实验中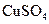 溶液起相似作用的是;
溶液起相似作用的是;
(4)要加快上述实验中气体产生的速率,还可采取的措施有(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 |
A |
B |
C |
D |
E |
F |
| 4mol/LH2SO4/mL |
30 |
V1 |
V2 |
V3 |
V4 |
V5 |
| 饱和CuSO4溶液/mL |
0 {007} |
0.5 |
2.5 |
5 |
V6 |
20 |
| H2O/mL |
V7 |
V8 |
V9 |
V10 |
10 |
0 |
①请完成此实验设计,其中:V1=,V6=,V9=;
②该同学最后得出的结论为:当加入少量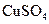 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的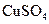 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因。
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因。
苯是一种重要的化工原料,也是一种重要的溶剂。请回答下列问题:
⑴把苯加入到盛有溴水的试管中,液体会出现分层现象,充分振荡、静置,出现橙红色液体的一层在层(填“上”或“下”);
⑵把苯加入到盛有少量高锰酸钾溶液的试管中,振荡后,酸性高锰酸钾溶液不褪色,说明苯分子中(填“有”或“没有”)碳碳双键;
⑶在浓硫酸作用下,苯在50~60℃可以与浓硝酸反应生成硝基苯,反应的化学方程式为。
已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的阳离子核外电子数为零,B原子的最外层电子数是内层电子数的2倍。C、D在元素周期表中处于左右相邻的位置,它们的单质是空气的主要成分, E元素与D元素同主族。
(1) 请写出元素符号:A_______, E______。
(2) C的气态氢化物的水溶液呈_______ 性(填“酸”、“碱”或“中”),写出C的气态氢化物的电子式_____________,以及与HCl形成的盐的化学式______________ 。
⑶A、B两元素形成的相对分子质量最小的有机物的分子式,空间构型是。
A是面粉中的主要成分,C与E反应可生成F,D能与新制的Cu(OH)2悬浊液反应产生砖红色沉淀。下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图: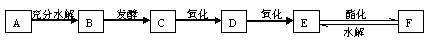
根据以上信息完成下列各题:
(1)A的化学式为____________,B的名称为_____________。
(2)C的结构简式为__________,D的结构简式为__________,F的结构简式为__________。
(3)C和E反应生成F的化学方程式为_________________________________。
(4)E与小苏打溶液反应的化学方程式为_______________________________________。