著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法不正确的是 ( )
| A.铈的冶炼步骤为:用稀土串级萃取法对矿石进行筛选富集;电解熔融CeO2。 |
| B.CeO2溶于氢碘酸的化学方程式可表示为:CeO2+4HI=CeI4+2H2O |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+ |
D.四种稳定的核素 、 、 、 、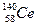 、 、 ,它们互称为同位素 ,它们互称为同位素 |
以下说法正确的是()
| A.纳米材料是一种称为“纳米”的新物质制成的材料 |
| B.绿色食品是指不含任何化学物质的食品 |
| C.生物固氮是指植物通过叶面直接吸收空气中的氮气 |
| D.光导纤维是以二氧化硅为主要原料制成的 |
水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
| A.水由液态变为玻璃态,体积缩小 |
| B.水由液态变为玻璃态,体积膨胀 |
| C.玻璃态水中氢键与冰不同 |
| D.玻璃态水是分子晶体 |
该晶体的晶体类型:()
| A.离子晶体 | B.分子晶体 | C.原子晶体 | D.金属晶体 |
若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则
天然气水合物的平均组成可表示为
| A.CH4·14H2O | B.CH4·8H2O |
| C.CH4·(23/3)H2O | D.CH4·6H2O |
下列关于天然气水合物中两种分子极性的描述正确的是
| A.两种都是极性分子 |
| B.两种都是非极性分子 |
| C.CH4是极性分子,H2O是非极性分子 |
| D.H2O是极性分子,CH4是非极性分子 |