铜和镁的合金2.14g完全溶于一定浓度的硝酸,若反应中硝酸被还原为NO2、NO、N2O三种气体且标准状况下体积均为0.224L,在反应后的溶液中,加入足量的氢氧化钠溶液,生成的沉淀经过滤.洗涤.干燥后称量,质量为 ( )
| A.3.12g | B.4.18g | C.4.68g | D.5.08g |
已知H2R为二元弱酸:H2R HR-+H+ Ka1 HR-
HR-+H+ Ka1 HR- R2-+H+ Ka2
R2-+H+ Ka2
常温下,向某浓度的H2R溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2R、HR-、R2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是
| A.pH=1.2溶液中:c(K+) + c(H+) = c(OH-) + c(H2R) |
| B.pH=2.7溶液中:c2(HR-) / [c(H2R) × c(R2-)]= 1000 |
| C.将相同物质的量KHR和K2R固体完全溶于水可配得pH为4.2的混合液 |
| D.向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离程度一直增大 |
实验室可利用硫酸厂炉渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4•7H2O),聚铁的化学式为[Fe2(OH)n(SO4)3﹣0.5n]m,制备过程如图所示:下列说法不正确的是
| A.炉渣中FeS与硫酸和氧气的反应的离子方程式为:4FeS+3O2+12H+═4Fe3++4S↓+6H2O |
| B.气体M的成分是SO2,通入双氧水得到硫酸,可循环使用 |
| C.溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏大 |
| D.向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸发浓缩、冷却结晶、过滤等步骤得到绿矾 |
对于反应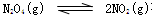 在温度一定时,平衡体系中NO2的体积分数(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是
在温度一定时,平衡体系中NO2的体积分数(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是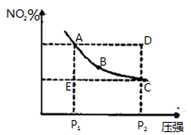
A.A、C两点的正反应速率的关系为A C
C
B.A、B、C、D、E各状态中,v(正)<v(逆)的是状态E
C.维持P1不变,E→A所需时间为x;维持P2不变,D→C所需时间为y,则x<y
D.使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是从P1突然加压至P2,再由P2无限缓慢降压至P1
在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是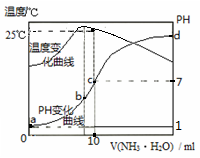
| A.a点KW=1.0×10-14 |
| B.水的电离程度:b>c>a>d |
| C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| D.25℃时,一水合氨的电离平衡常数为10-7/(10n-1)(用n表示) |
下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/ c(HCO3-)的比值保持增大
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO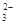 )+c(HCO
)+c(HCO )]
)]
③在0.1 mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH)=l0-a mol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)-c(H2S)-c(HS-)
| A.①④ | B.②⑤ | C.①③ | D.②④ |