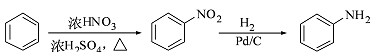
蓝铜矿主要含2CuCO3·Cu(OH)2,还含有少量Fe、Si的化合物,工业上以蓝铜矿为原料制备Cu及CaCO3,方法有多种。
(1)蓝铜矿与焦炭加热可以生成铜、二氧化碳和水,写出该反应的化学方程式。______________________________________________________________。
具体方法步骤如下: 
请回答下列问题:
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:检验溶液A中含有Fe2+的最佳试剂为 (填代号),实验步骤中试剂①为 (填代号)。
a.KMnO4 b.(NH4) 2S c.H2O2 d.KSCN
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,冷却结晶、过滤等操作,加热蒸发至 ___________________时停止加热。玻璃棒在整个操作中的作用是 ________________ 。
(4)制备CaCO3时,应向CaCl2溶液中先通入(或先加入) (填化学式)。若实验过程中有氨气逸出、应选用下列 装置吸收尾气(填代号)。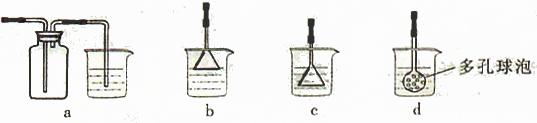
(5)从溶液C中获得Cu的方法有 (写出两种不同方法)。
(6)用惰性电极电解硫酸铜溶液一段时间后,加入2molCu(OH)2固体使硫酸铜溶液复原(复原是指溶液溶质成分及浓度与原来完全相同),则此电解过程中共转移电子 mol。
常温下,将a mL 三种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 |
c(一元酸) |
c(NaOH) /mol/L |
混合溶液的pH |
| 甲 |
c(HX)=0.1 mol/L |
0.1 |
pH = x |
| 乙 |
c(HY)=0.1mol/L |
0.1 |
pH = 7 |
| 丙 |
c(HZ)=0.1 mol/L |
0.1 |
pH = 9 |
(1)上述三种酸中一定属于强酸的是___________;
(2)丙组实验发生反应的离子方程式为,所得溶液中由水电离出的c(OH-) =mol/L;
(3)甲组中x的值_____7(填>、<、=);
(4)部分实验反应过程中的pH变化曲线如下图:
①表示乙组实验的pH变化曲线是________________
②上图中表示溶液呈中性的点为_________,表示溶液恰好完全反应的点是_______
③E点对应离子浓度由大到小的顺序为。
在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g)+Q(Q>0),
2NH3(g)+Q(Q>0),
(1)该反应所用的催化剂是 (填写名称)
该反应450℃的平衡常数 500℃时的平衡常数(填“>”、“<”或“=”)。
(2)下列描述中能说明上述反应已达平衡的是
| A.3V正(H2)=2V逆(NH3) | B.容器中气体的平均分子量不随时间而变化 |
| C.容器中气体的密度不随时间而变化 | D.容器中气体的分子总数不随时间而变化 |
(3)如上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为______________mol/(L¯min)。
(4)下列研究目的和示意图相符的是 。
| A |
B |
C |
D |
|
| 研究目的 |
压强对反应的影响(P1>P2) |
温度对反应的影响 |
平衡体系增加N2对反应的影响 |
催化剂对反应的影响 |
| 图示 |
 |
 |
 |
 |
以下反应①②可用于从不同原料中提取碘:
①2NaI+MnO2+3H2SO4 2NaHSO4+MnSO4+2H2O+I2
2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3 2Na2SO4+3NaHSO4+H2O+I2
2Na2SO4+3NaHSO4+H2O+I2
(1)反应①中的氧化剂是___________________;反应②中的还原产物是________________。
(2)根据反应①②可推知______。
a.氧化性:IO3->SO42-b.氧化性:MnO2>NaIO3
c.还原性:I->Mn2+d.还原性:I2>NaHSO3
(3)已知NaI和NaIO3在酸性条件下能反应生成I2 ,写出该反应的离子方程式:
③__________________________________________________________。
(4)三个反应中生成等量的I2时转移的电子数最少的是反应________(填序号)。
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
CH4(g)+2NO2 (g)=N2(g) + CO2(g)+2H2O(g)△H3=-867kJ·mol-1
则△H2=。
Ⅱ. 化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为C(s) + H2O(g)= CO(g) + H2(g),
该反应的化学平衡常数表达式为K=。 800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应:CO(g) + H2O(g)  CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如图t2后所示的变化,则改变的条件可能是(填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如图t2后所示的变化,则改变的条件可能是(填符号)。
a加入催化剂b降低温度c缩小容器体积d减少CO2的量
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
①用离子方程式表示反应器中发生的反应。
②用化学平衡移动的原理分析,在 HI分解反应中使用膜反应器分离出H2的目的是。
Ⅲ.开发新能源是解决大气污染的有效途径之一。甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:
通入a气体的电极是原电池的极(填“正”或“负”),其电极反应式为。
卤代烃(R—X)在醚类溶剂中与Mg反应可制得格氏试剂,格氏试剂在有机合成方面用途广泛。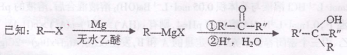
(R表示烃基,R′和 R”表示烃基或氢)
现某有机物A有如下转化关系:
试回答下列问题:
(1)B→C的反应类型是。
(2)B→A的化学反应方程式是。
(3)G的结构简式是。
(4)I中所含官能团的名称是。
(5)写出一种满足下列条件的物质I的同分异构体的结构简式。
①能发生银镜反应;②核磁共振氢谱有3个峰; ③拥有最多的甲基
(6)聚苯乙烯(PS)是一种多功能塑料,广泛应用于食品包装,绝缘板,商业机器设备等许多日常生活领域中。写出以 D和苯为主要原料制备聚苯乙烯的合成路线流程图(无机试剂任选)。合成路线流程图示例如下: