下列装置或操作不能达到实验目的的是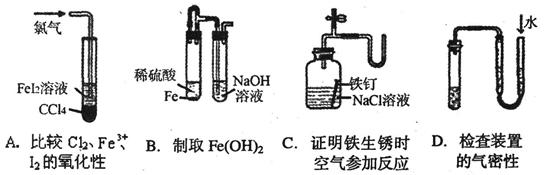
对于下列反应类型的判断,不正确的是 ( )
| A.2FeCl2+Cl2====2FeCl3(化合反应) |
B.3CO+Fe2O3 2Fe+3CO2(置换反应) 2Fe+3CO2(置换反应) |
C.2KClO3 2KCl+3O2↑(氧化还原反应) 2KCl+3O2↑(氧化还原反应) |
D.H2CO3 CO2↑+H2O(分解反应) CO2↑+H2O(分解反应) |
下列说法正确的是 ( )
| A.无氧酸是指分子组成中不含氧元素的酸,如HCl、CH4等 |
| B.根据溶解性的不同,可将碱分为难溶性碱和可溶性碱 |
| C.和酸反应生成盐和水的物质一定是碱性氧化物 |
| D.所有的酸性氧化物都可以与水化合得到相应的酸 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol· L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是()
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
恒温下,在容积为1升的甲、乙两个恒容密闭容器中分别充入H2和I2发生可逆反应:H2(g)+I2(g)⇌2HI(g)△H=-14.9kJ/mol,实验时有关数据如表:
| 容器编号 |
起始浓度mol/L |
平衡时的浓度mol/L |
平衡时放出的热量/KJ |
|
| I2 |
H2 |
HI |
||
| 甲 |
0.01 |
0.01 |
0.004 |
Q1 |
| 乙 |
0.02 |
0.02 |
a |
Q2 |
下列判断正确的( )
A.平衡时,乙中颜色更深,a>0.008
B.平衡时,放出的热量:Q1=1/2Q2=0.149kJ
C.该温度下,该反应的平衡常数K=4
D.平衡后,向甲中再充入0.004molHI气体,再次达到平衡时HI的百分含量不变
常温下,下列溶液中有关物质的量浓度关系和计算不正确的是()
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:
c(NH4Cl) ﹥c[(NH4)2SO4]﹥c[(NH4)2Fe(SO4)2]
B.已知25°C时Ksp(AgCl)=1.8×10-10,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol·L-1
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH约为1
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有C(HA-) >C(H+)>C(A2-)>C(H2A)