25℃时,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下表:
| 物质 |
AgCl |
AgI |
Ag2S |
| 颜色 |
白 |
黄 |
黑 |
| Ksp(25℃) |
1.8×10-10 |
1.5×10-16 |
1.8×10-50 |
下列叙述中不正确的是
| A.溶度积小的沉淀可以转化为溶度积更小的沉淀 |
| B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生 |
| C.25℃时,AgC1固体在等体积、等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 |
| D.25℃时,AgC1固体在等体积、等物质的量浓度的NaCl、CaCl2溶液中的c(Ag+)相同 |
一定量的某有机物完全燃烧后,生成1 mol CO2和9 g H2O,该有机物可能是
| A.C3H8 | B.CH3CH2OH | C.CH3CHO | D.C2H2 |
短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为20。则下列说法不正确的是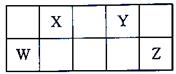
| A.最高价氧化物的水化物的酸性:X<Z |
| B.原子半径大小:Y<X<W |
| C.氢化物的稳定性X<Y |
| D.X和Y形成的化合物升华破坏的是共价键 |
相同温度和压强下,在容积为2 L的密闭容器中发生反应:2HI(g)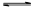 H2(g)+I2(g),达到平衡状态的标志是
H2(g)+I2(g),达到平衡状态的标志是
| A.c(H2)保持不变 |
| B.拆开2 mol H-I共价键,同时生成1 mol H-H共价键 |
| C.HI、H2、I2的浓度比为2:1:1 |
| D.正反应和逆反应都已停止 |
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为:2Zn+O2=2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是
| A.锌为正极,空气进入负极反应 |
B.负极反应为:Zn-2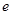 -=Zn2+ -=Zn2+ |
| C.正极发生氧化反应 |
D.正极反应为: Zn-2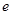 -=Zn2+ -=Zn2+ |
在25℃,101 k Pa下,0.2 mol C2H2完全燃烧生成CO2和H2O(l)时放出259.92 kJ热量。表示上述反应的热化学方程式正确的是
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g) △H=+259.92 kJ/mol |
| B.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-259.92 kJ/mol |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=+2599.2 kJ/mol |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2599.2 kJ/mol |