.在实验室做用锌与某浓度的盐酸起反应的实验中,一个学生得到下面的结果
| 序号 |
锌的质量(g) |
锌的形状 |
温度(℃) |
完全溶 解于酸的时间(s) 解于酸的时间(s) |
| A |
2 |
薄片 |
5 |
400 |
| B |
2 |
薄片 |
15 |
200 |
| C |
2 |
薄片 |
25 |
100 |
| D |
2 |
薄片 |
30 |
t1 |
| E |
2 |
薄片[ |
35 |
50 |
| F |
2 |
颗粒 |
15 |
t2 |
| G |
2 |
粉末 |
15 |
t3 |
①t1=75 ②t2>200>t3 ③单位时间内消耗的锌的质量m(C)>m(B)>m(G)
则下列说法正确的是 ( )
A.①③ B.①② C.只有② D.全部正确
碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可以作家用洗涤剂,如清洗厨房用具的油污等。下列不能将加碘食盐和碳酸钠区别开的试剂或用品是
A.食醋 |
B.淀粉 |
C.pH试纸 | D.酚酞试液 |
下列说法正 确的是
确的是
| A.摩尔质量就等于物质的式量 | B.摩尔质量是物质式量的6.02×1023倍 |
| C.HNO3的摩尔质量是63g | D.氧化铜和三氧化硫的摩尔质量相等 |
下列叙述与胶体的性质无关的是

| A.同一支钢笔使用不同品牌墨水时,容易发生堵塞现象 |
| B.当日光从窗隙射入暗室时,可观察到一束光线 |
| C.向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 |
| D.肾功能衰竭等疾病引起的尿毒症,可利用血液透析进行治疗 |
在标准状况下,如果2.8L氧气含有 个氧原子,则阿伏伽德罗常数为
个氧原子,则阿伏伽德罗常数为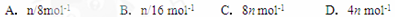
当光束通过下列分散系:① 尘埃的空气 ② 稀硫酸 ③ 蒸馏水 ④ 墨水, 能观察到有丁达尔现象的是
| A.①② | B.②③ | C.①④ | D.②④ |