在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(1)阳极上的电极反应式为__________________________。
(2)阴极上的电极反应式为______________________________。
(3)原上层液体是_______________________________________。
(4)原下层液体是________________________________________。
(5)搅拌后两层液体颜色发生变化的原因是_____________________
______________________________________________________________________________。
(6)要检验上层液体中含有的金属离子,其方法是__________________________,
现象是_____________________________________________________________。
应用化学反应原理知识解决下列问题
(1)某温度下纯水中c (H+) = 2.0×10-7 mol·L-1,则此纯水中的c (OH-) =。
(2)将某CH3COOH溶液稀释10倍,则稀释后的溶液中c(H+)原来的十分之一(填“大于”、“小于”或“等于”)。
(3)0.1 mol·L-1的下列溶液①HCl、②CH3COOH、③CH3COONa、④FeCl3、⑤NaOH,其中pH最大的是(填序号);实验室配制的氯化铁溶液显弱酸性的原因:(用离子方程式表示)。
(4)一定条件下22g二氧化碳气体与足量氢气反应生成气态甲醇(CH3OH)和水蒸气时,放出247.5kJ热量,其反应的热化学方程式为。
浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:。
(2)实验室用二氧化锰制取氯气的化学方程式为:;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气(填写装置的序号)。
(3)实验室中模拟Br—→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br—→Br2的转化离子方程式为:;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是(选填下列选项的编号字母)。
(4)实验室制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100 mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如右图),再把已称好50.0 g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应。观察读数变化如下表所示:
| CaCO3用量 |
未加CaCO3时 |
加约四分之一时 |
加一半时 |
全部加完时 |
| 读数/g |
318.3 |
325.3 |
334.5 |
359.5 |
请你据此分析计算:
①实验中产生的CO2气体质量为;
②残余液中盐酸的物质的量浓度为 (结果精确到小数点后一位)。
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________ (填序号)。
①单质②氧化物③电解质④盐⑤化合物
(2)现有铜、氯化铁溶液、盐酸、硝酸银溶液、氧化铝、二氧化碳、氧气七种物质,两两能发生反应的反应中,属于离子反应的有种,属于置换反应的有种。
化学反应原理在科研和生产中有广泛应用。
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:
TaS2(s)+2I2(g) TaI4(g)+S2(g) (Ⅰ)
TaI4(g)+S2(g) (Ⅰ)
某温度反应(Ⅰ)的K=4,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为 。
(2)如下图所示,反应(Ⅰ)在石英真空管中进行,先在温度高(T2)的一端放入未提纯的TaS2粉末和少量I2(g),加热一段时间后,在另一端温度低(T1)的一端得到了纯净的TaS2晶体,则该正反应的△H0(填“>”或“<”),上述反应体系中循环使用的物质是。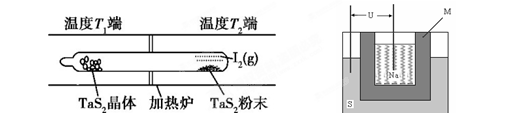
(3)上图为钠硫高能电池的结构示意图。该电池的工作温度为320℃左右,电池反应为2Na + xS=Na2Sx,正极的电极反应式为____________________________。M(由Na2O和Al2O3制得)的两个作用是________________________________________________和隔离钠与硫。
(4)写出Na2S溶液水解的离子方程式_______________________________________,Na2S溶液中c(H+)+ c(Na+)=________________。
(1)常温下,将NH3·H2O与盐酸等体积混合,实验数据如下:
| 组别 |
NH3·H2O |
HCl |
混合溶液的pH值 |
| 甲 |
c(NH3·H2O)=0.1mol·L-1 |
c(HCl)=0.1mol·L-1 |
pH=a |
| 乙 |
NH3·H2O的pH=12 |
HCl的pH=2 |
pH=b |
| 丙 |
c(NH3·H2O)="A" mol·L-1 |
c(HCl)=0.1mol·L-1 |
pH=c |
针对甲、乙、丙三组实验,回答下列问题:
①甲组反应后,溶液中离子浓度的大小顺序为__________________;
②乙组b7(填“>”、“<”或“=”)
③丙组溶液混合后c=7,A0.1mol·L-1(填“>”、“<”或“=”)
④甲中a=6,混合溶液中c(Cl-)-c(NH4+)= ____________mol·L-1 (列式表示结果,不能做近似计算)。(2)常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸。溶液的PH 的变化关系如右图所示。
①a >7.0的理由是(用离子方程式表示)。
②当加入的盐酸的体积为20.0mL时,测定溶液中的c(H+)为1.3×10-3 mol/L,求CH3COOH的电离平衡常数Ka(设混合后的体积为二者的体积之和,计算结果保留两位有效数字。)