【化学—选修3 物质结构与性质】
A、B、C、D、E是原子序数逐渐增大的1-36号元素。A原子核外有4个原子轨道填充了电子;B的第一电离能比同周期相邻元素的第一电离能大,其气态氢化物在水中的溶解度在同族元素氢化物中最大;C的最高化合价和最低化合价的代数和为4;D原子的M层和N层电子数均比E原子少4个,E是人体必须的微量元素。
试根据 以上信息,回答下列问题:
以上信息,回答下列问题:
(1)A原子的电子排布图 ,E原子的外围电子排布式为 。
(2)AC2分子中含有 个π键。
(3)含C50%的C的氧化物的空间构型为_________,C的原子轨道采用______杂化。
(4)写出A的常见氧化物与B的氧化物中互为等电子体的一组 。
(5)已知D的晶体在不同温度下有A、B两种堆积方式,则A、B两晶胞中D原子的配位数之比 ; 晶体的密度之比为 。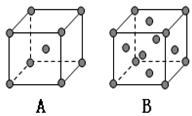
写出下列反应的化学方程式。
(1)检验乙醇中是否混有乙醛:
(2)由丙烯制聚丙烯:
(3) 制取TNT:
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A的最高价氧化物对应的水化物是_______(填化学式);
(2)物质E中所包含的化学键有________,写出C、D两元素形成的化合物C2D的电子式_________;
(3)在同主族氢化物的递变性质中,A的氢化物沸点反常,这可以用解释。
A.共价键 B.离子键 C.氢键 D.范德华力
(4)与C同主族且处于第七周期的元素的原子序数是.
(5)把盛有48 mL AB、AB2混合气体的容器倒置于水中(同温、同压下),待液面稳定后,容器内气体体积变为24 mL,则原混合气体中AB的体积分数为_______ 。
短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
已知: a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲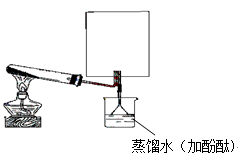
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中的试剂是(填写化学式)。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是。
(4)nmol丁与nmol丙在一定条件下反应,生成4nmol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是_ ___。
在一定条件下,向体积为2 L的容器中加入2 mol O2和3 mol SO2使之反应生成SO3气体:2SO2+ O2 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
(1)2min内,平均反应速率v(O2)=; v(SO3)=。
(2)2min时,SO2的浓度为
(3)若2min时测得上述反应放出Q kJ的热量,试写出该反应的热化学方程式
现有①BaCl2②金刚石③KOH④H2SO4⑤干冰⑥碘片⑦晶体硅⑧金属铜八种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是________,熔化时需要破坏共价键的是________,熔点最高的是________,熔点最低的是________。
(2)属于离子化合物的是________,只有离子键的物质是________,晶体以分子间作用力结合的是________。
(3)①的电子式是________,⑤的电子式是________。