下列叙述中正确的是:( )
| A.原子晶体中,共价键的键能越大,熔沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中属于这种情况的是
①过量的锌与18 mol·L-1的硫酸反应
②过量的氢气与少量氮气在一定温度、压强和催化剂存在下充分反应
③加热条件下浓盐酸与过量的MnO2反应
④加热条件下过量铜与浓硫酸反应
⑤过量稀硫酸与块状石灰石反应
| A.②③④⑤ | B.②③④ | C.①③④ | D.①②③④⑤ |
下列变化只需通过一步化合反应就可以实现的是
| A.FeCl3→FeCl2 | B.Al2O3→Al(OH)3 |
| C.SiO2→H2SiO3 | D.S→SO3 |
溶液中含有NO3-、SO32-、Cl-和NH4+,若向其中加入足量的盐酸,溶液里上述四种离子的浓度基本保持不变的是
| A.NO3- | B.SO32- | C.Cl- | D.NH4+ |
已知A、B、C、D四种物质中均含同种元素,且它们之间的转化关系如下。下列说法正确的是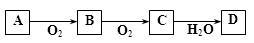
A.A一定为单质
B.C一定为氧化物
C.D一定为酸
D.A、B、C的相对分子质量之差为16或16的倍数
下列实验能达到预期目的的是
| A.检验溶液中是否含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 |
| B.检验溶液中是否含有SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
| C.检验溶液中是否含有Fe2+:先滴加氯水,再滴加KSCN溶液 |
| D.检验溶液中是否含有NH4+:先滴加浓NaOH溶液并加热,再用湿润的红色石蕊试纸 |