在接触法制硫酸的有关问题中,下列叙述不正确的是
A.燃烧黄铁矿制取SO2的化学方程式是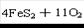  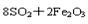 |
| B.含SO2的炉气在进行氧化反应前必须净化,其目的就是为了除尘、以防催化剂中毒 |
| C.用98.3%的浓H2SO4吸收SO3制取发烟硫酸,用稀H2SO4吸收SO3制较浓的H2SO4 |
| D.SO2氧化时必须使用催化剂(例如V2O5等),催化剂的作用是提高SO2的氧化速率,缩短到达平衡所需的时间,但使用催化剂不会提高SO2的转化率 |
有一反应:2A+B 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是()
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是()
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下若由a点达到平衡,可以采取增大压强的方法
D.c点:v(正)<v(逆)
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)  4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是()
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是()
| A.前2 min,D的平均反应速率为0.2 mol/(L·min) |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,平衡不移动 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
| T/K |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1 173 |
2.15 |
1.67 |
下列有关叙述正确的是()
A.b<0
B.在973 K下增大压强,K2增大
C.a>b
D.在常温下反应①一定能自发进行
将4 mol A和2 mol B放入2 L密闭容器中发生反应:2A (g)+B(g)2C(g);ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是()
A.4 s内,v(B)=0.075 mol/(L·s)
B.4 s后平衡状态下,c(A)∶c(C)=2∶1
C.达到平衡状态时,若只升高温度,则C的物质的量浓度增大
D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)  SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是()
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是()
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |