荧光素是发光物质的基质,5-羧基荧光素与5-羧基荧光素二乙酸酯在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
下列说法正确的是
A.5-FAM转变为5-CFDA属于取代反应
B.实验室鉴别5-FAM与5-CFDA可用碳酸氢钠溶液
C.5-FAM的分子式为:C21H3O7
D.5-FAM和5-CFDA分子中的所有原子均共面
有机反应的类型很多,下列各反应中与CH2 CH2
CH2 CH2Br—CH2Br的变化属于同一反应类型的是 ( )
CH2Br—CH2Br的变化属于同一反应类型的是 ( )
A.C2H5Cl CH2 CH2 CH2 CH2 |
B.CH3CHO C2H5OH C2H5OH |
C.   |
D.CH3COOH CH3COOC2H5 CH3COOC2H5 |
下列各项中表达正确的是 ()
A.四氯化碳的电子式: |
B.CH4分子的比例模型  |
C.环己烷的结构简式 |
D.次氯酸的结构式: H—Cl—O |
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制得产物,即原子利用率100%。以下反应最符合绿色化学的是()
| A.乙醇与金属钠反应制取乙醇钠 | B.CH4与Cl2反应制取CCl4 |
| C.苯与液溴反应制取溴苯 | D.CH2=CH2与HCl反应制取CH3CH2Cl |
居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料会释放出一种刺激性气味的有机气体,它对人体极为有害。该气体是 ()
| A.甲烷 | B.甲醛 | C.氨气 | D.二氧化硫 |
第二十九届奥林匹克夏季运动会于2008年8月8日—24日在北京隆重举行并获得巨大成功。下图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃。下列说法正确的是()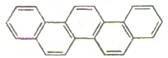
| A.该有机物的一氯代物只有一种 |
| B.该有机物是只含非极性键的非极性分子 |
| C.该有机物属于芳香族化合物,不是苯的同系物 |
| D.该有机物完全燃烧生成H2O的物质的量大于CO2的物质的量 |