甲烷中混有另一种或几种气态烃所组成的混合物1 L,完全燃烧需同温同压下的O2 3 L,并测得该气态烃混合物对氢气的相对密度为12.67,那么甲烷中可能混入的气态烃是
| A.CnH2n+2(n>1) | B.CnH2n(n>2) |
| C.CnH2n(n>1)和CmH2m(m>2) | D.CnH2n-2(n>1)与CmH2m-2(m,n>1) |
下列事实与推论相符的是
| 选项 |
实验事实 |
推论 |
| A |
H2O的沸点比H2S的沸点高 |
非金属性:O>S |
| B |
盐酸的酸性比H2SO3的酸性强 |
非金属性:Cl>S |
| C |
钾与水的反应比钠与水的反应更剧烈 |
金属性:Na>K |
| D |
HF的热稳定性比HCl的强 |
非金属性: F>Cl |
下列说法中不正确的是
①质子数相同的粒子一定属于同一种元素
②同位素的性质几乎完全相同
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素的原子
⑤一种元素不可以形成不同的单质
⑥某种元素的相对原子质量取整数,就是其质量数
| A.①②⑤⑥ | B.①②④⑤ | C.②③⑤⑥ | D.③④⑤⑥ |
运用元素周期律分析下列推断,其中错误的是
| A.铍是一种轻金属,它的氧化物的水化物可能具有两性 |
| B.砹单质是一种有色固体,砹化氢很不稳定 |
| C.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
| D.硫酸锶难溶于水 |
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素大厦”中安排好它的“房间”
| A.第七周期0族 | B.第八周期第ⅠA族 |
| C.第六周期第ⅡA族 | D.第七周期第ⅦA族 |
一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
2NH3(g) ΔH<0,反应过程如图,下列说法正确的是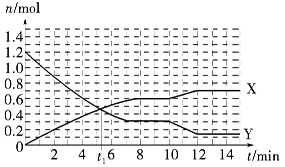
| A.t1 min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
| C.0~8 min,H2的平均反应速率v(H2)=0.01mol·L-1·min-1 |
| D.10~12 min,升高温度使反应速率加快,平衡正向移动 |